Растворимость - магний
Cтраница 2
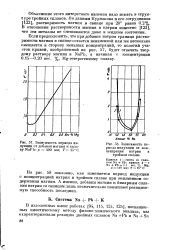 |
Зависимость периода индукции от добавок магния к сплаву NaP b. p 400 мм. Т 35 С.| Зависимость периода индукции от кон - центрации натрия в тройном сплаве. [16] |
Если предположить, что при добавке натрия граница растворимости магния в свинце остается неизменной или же несколько смещается в сторону меньших концентраций, то пологий участок кривой, изображенной на рис. 57, будет отвечать твердому раствору магния в NaPb, а начиная с концентрации 0.15 - 0.20 вес. [17]
Добавки хлоридов щелочных металлов, с одной стороны, понизили растворимость магния в расплаве хлорида магния с этими добавками, а с другой - понизили и выход по току. Причиной, снижающей выход по току магния в присутствии добавок хлоридов щелочных металлов, является, по-видимому, разряд на катоде более электроотрицательных по сравнению с магнием катионов. При небольшом содержании в расплаве добавок NaCl и КС1 выделение К и Na на катоде происходит в незначительной степени. [18]
Магний образует с алюминием обширную область твердых растворов ( рис.); растворимость магния в алюминии при эвтектич. [19]
Кроме того, добавление хлоридов натрия, калия и кальция к хлориду магния снижает растворимость магния в нем. [20]
Это, как видно, связано с тем, что при повышении концентрации этих добавок в электролите растворимость магния падает и возможность разряда других ионов на катоде ( К, Na, Baa) возрастает; выход но току, конечно, увеличивается с повышением содержания MgCl2 в расплаве. [21]
Добавка до 0 15 % Zr в тройной сплав, близкий по составу к описанному выше, понижает растворимость магния и лития в алюминии. Поэтому в отличие от композиций с марганцем после закалки от 450 С в структуре полуфабрикатов сохраняется большее количество нерастворенных частиц, по-видимому, равновесных соединений алюминия с магнием и литием размером 0 1 - 0 3 мкм. Растворение частиц происходит при 500 - 540 С. [22]
 |
Предел прочности сплавов ( кГ / мм2 А1 - Zn - Mg ( 0 4 % Mn. 0 2 % Сг после закалки и старения ( 140 С, 16 ч. [23] |
С в течение 16 ч) прочность сплавов растет по мере увеличения концентрации магния и цинка в твердом растворе, поскольку растворимость магния в алюминии уменьшается с увеличением содержания в нем цинка, максимум прочности сдвигается в сторону снижения количества магния. Сплавы, расположенные в области a - MgZn2 и а Т, имеют примерно одинаковый максимальный уровень прочности. [24]
В отношении растворимости магния в натрии известно [123], что эти металлы не смешиваются даже в жидком состоянии. [25]
Согласно диаграмме состояния А1 - Mg ( фиг. С понижением температуры растворимость магния в твердом алюминии уменьшается и при 20 становится равной 1 95 % - Это обстоятельство указывает на то, что магналий должен был бы в результате закалки и старения упрочниться. [26]
С увеличением температуры электролита выше 750 потери металла резко возрастают. Это объясняется повышением растворимости магния в электролите, обусловленном возрастанием упругости паров магния с температурой. [27]
С увеличением давления на уровне наконечника ( столб жидкости в за-трубном пространстве) скорость реакции кислоты с магнием сильно замедляется. Ниже приводятся данные о растворимости магния в растворе соляной кислоты 15 % - ной концентрации с увеличением давления. [28]
Описанная выше схема электролиза осложняется рядом побочных процессов, снижающих выход по току, загрязняющих хлор, разрушающих материалы анода и футеровки электролизера и приводящих к образованию шлама. К таким побочным явлениям относятся главным образом растворимость магния в электролите, взаимодействие его с анодным хлором, кислородом воздуха на поверхности электролита и с вредными примесями в электролите - влагой, солями железа и сульфатами. [29]
Описанная выше простая схема электролиза осложняется рядом побочных процессов, снижающих выход по току, загрязняющих хлор, разрушающих материалы анода и футеровки ванны и приводящих к образованию шлама. К таким побочным явлениям относятся главным образом растворимость магния в электролите взаимодействие его с анодным хлором, кислородом воздуха на поверхности электролита и с вредными примесями в электролите - влагой, солями железа и сульфатами. [30]
Страницы: 1 2 3