Растворимость - неполярный газ
Cтраница 2
Уравнение ( 59), как следовало ожидать, позволяет с хорошей точностью рассчитывать растворимость неполярных газов только в неполярных или так называемых нормальных жидкостях, и оказывается мало пригодным для полярных растворителей. Ошибки в вычислении по уравнению ( 59) растворимости газов в воде превышают разумные пределы. [16]
Вторая стадия растворения, обусловленная силами межмолекулярного взаимодействия, зависит от строения молекул растворяемого вещества и растворителя. В табл. 7.2 были приведены некоторые данные по растворимости различных газов в воде. Растворимость неполярных газов Н2, N2, O2 ( л О) в воде очень мала, так как между ними и полярными молекулами воды могут возникать лишь дисперсионные силы взаимодействия, что приводит к малой энергии связи. Молекулы диоксида углерода СО2 ( j, 0) обладают полярными связя-ми и при взаимодействии с молекулами воды могут приобрести большой индуцированный электрический момент - растворимость СО2 в воде значительная. [17]
Вторая стадия растворения, обусловленная силами межмолекулярного взаимодействия, зависит от строения молекул растворяемого вещества и растворителя. В табл. 34 были приведены некоторые данные по растворимости различных газов в воде. Растворимость неполярных газов Н2, N2, О2 ( ц0) в воде очень мала, так как между ними и полярными молекулами воды могут возникать лишь дисперсионные силы взаимодействия, что приводит к малой энергии связи. Молекулы двуокиси углерода С02 ( ц 0) обладают полярными связями и при взаимодействии с молекулами воды могут приобрести большой индуцированный дипольный момент - растворимость СО2 в воде значительная. [18]
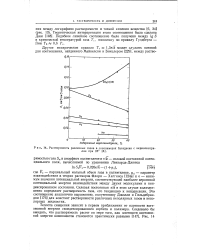 |
Растворимость различных газов в сополимерах бутадиена с акрилонитри. [19] |
Силовая постоянная e / k в этом случае количественно определяет растворимость газа, его тенденцию к конденсации. Это соотношение аналогично выражению, полученному Джолли и Гильдебран-дом [176] для констант растворимости различных неполярных газов в неполярных жидкостях. [20]
Если в смеси газов, один из компонентов которой присутствует в подавляющем количестве, все газы неполярные ( они же малорастворимые), то растворимостью в воде всех компонентов кроме основного можно обычно пренебречь. Это вызвано тем, что растворимость в воде упомянутых газов в десятки раз выше растворимости неполярных газов. [21]
Страницы: 1 2