Кривая растворимость
Cтраница 1
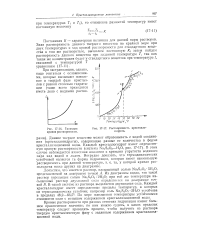 |
Типичная кривая растворимости.| Растворимость кристаллогидрата. [1] |
Кривые растворимости при разных степенях гидратации имеют большое практическое значение; по ним можно судить, в каких пределах температур следует проводить процесс, чтобы получить из раствора твердую кристаллическую фазу с заданным содержанием кристаллизационной воды. [2]
Кривые растворимости строят в координатах температура - состав раствора. Использование такого большого числа различных способов: выражения концентрации раствора часто затрудняет технологические расчеты процесса кристаллизации, а также его графическое изображение на диаграммах фазового равновесия. [3]
Кривые растворимости оказываются расположенными выше идеальной, кроме случаев образования твердых растворов, в системах в которых имеется тенденция к расслаиванию. Соответственно, системы трех упомянутых классов можно характеризовать различием коэффициентов активности насыщающего компонента: для систем первого класса коэффициенты активности близки к единице, второго - меньше, третьего - больше единицы. [4]
Кривые растворимости строят по экспериментально полученным данным. Диаграммы состояния водных или других растворов экстрагируемых веществ имеют важное практическое значение для балансовых расчетов в системах. Из многочисленных экстракционных систем большой интерес представляют водно-солевые системы, широко распространенные в природе и в химической промышленности. В этих системах участвуют химические соединения различных составов, прочности и устойчивости к внешним воздействиям. Образование химических соединений с различными типами химической связи должно характеризоваться постоянством состава. Такие соединения представляют собой: 1) твердые растворы, содержащие в каждом кристалле неодинаковые количества различных атомов ( ионов), которые неупорядоченно распределяются в пустотах между узлами кристаллической ре-щетки или замещают друг друга в узлах; 2) эвтектические смеси, плавящиеся при более низкой температуре, чем составляющие их вещества. Таким образом, существует три типа взаимодействия компонентов в системе, в результате чего образуются новые химические соединения ( обычно комплексные), эвтектические смеси или твердые растворы. Твердые растворы мешают получению компонентов в чистом виде. [5]
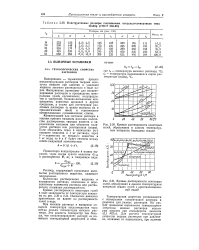 |
Конструктивные размеры поплавковых конденсатоотводчиков типа.| Кривые растворимости некоторых солей, образующих в данном температурном интервале безводные осадки.| Кривые растворимости некоторых. [6] |
Кривые растворимости некоторых солей в виде зависимости от температуры показаны на рис. 2.30 и 2.31. Изменение давления практически не влияет на растворимость солей в воде. [7]
 |
Кривые растворимости в воде некоторых солей. [8] |
Кривые растворимости показывают, как изменяется растворимость данного вещества с изменением температуры. [9]
Кривые растворимости некоторых солей изображены на диаграмме ( рис. 9), а в таблице ( см. Приложение) приведена растворимость солей в воде при различных температурах. [10]
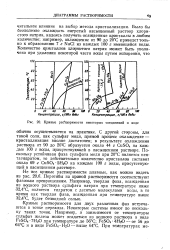 |
Кривые растворимости некоторых соединений в воде. [11] |
Кривые растворимости для двух различных фаз встречаются в точке перехода. Некоторые системы имеют по нескольку таких точек. [12]
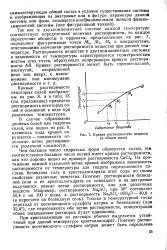 |
Кривая растворимссти веществ ( в общем виде. [13] |
Кривые растворимости некоторых солей изображены на рис. 8, а в табл. IX ( см. приложение) приведена растворимость некоторых солей и оснований в воде при различных температурах. [14]
Кривые растворимости некоторых солей изображены на диаграмме ( рис. 9), а в таблице ( см. Приложение) приведена растворимость солей в воде при различных температурах. [15]
Страницы: 1 2 3 4 5