Взаимная растворимость - вещество
Cтраница 2
Из неравенства ( 20) вытекает следующее правило: чем меньше взаимная растворимость веществ, тем более вероятно образование ими гетероазеотропа, так как он образуется при большем различии давлений паров компонентов. [16]
Одним из самых сложных вопросов физической химии является вопрос о причинах взаимной растворимости веществ. [17]
При обработке подлежащего экстрагированию водного раствора некоторым объемом выбранного растворителя извлекаемое вещество распределяется между водой и растворителем в соотношении, зависящем от взаимной растворимости вещества в каждой из жидкостей. Ясно, что однократная обработка не приводит к исчерпывающему извлечению целевого продукта. Обычно экстрагирование проводят последовательно несколькими небольшими порциями растворителя. [18]
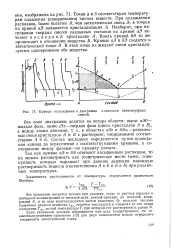 |
Кривые охлаждения и диаграмма плавкости неизоморфных. [19] |
Так как кривые аЭ и 6Э отвечают насыщенным растворам, то их можно рассматривать как геометрическое место точек, совокупность которых выражает при данном давлении взаимную растворимость веществ ( соответственно Л в Б и Б в Л) при различных температурах. [20]
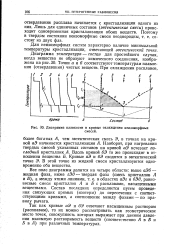 |
Диаграмма плавкости и кривые охлаждения неизоморфных. [21] |
Так как кривые аЭ 6Э отвечают насыщенным растворам ( расплавам), то их можно рассматривать как геометрическое место точек, совокупность которых выражает при данном давлении взаимную растворимость веществ ( соответственно Л в Б и Б в Л) при различных температурах. [22]
Взаимная растворимость веществ зависит от их химического строения. В качестве признака подобности впоследствии была принята близость энергии межмолекулярного взаимодействия. [23]
Карбамидную депарафинизацию проводят при 20 - 35 С. Повышение температуры увеличивает взаимную растворимость веществ, снижает их вязкость и улучшает условия контакта, однако стабильность комплексов и выход н-алканов при этом уменьшаются. Выбор температуры зависит от требуемой степени депарафинизации, пределов кипения исходной фракции и от того, вводится ли карбамид в кристаллическом состоянии или в виде водного раствора. Депарафинизацию сравнительно низкокипящих фракций, а также процесс с использованием водных растворов карбамида для повышения стабильности комплексов необходимо проводить при более низкой температуре. [24]
Согласно молекулярной теории растворов [74], состояние системы определяется двумя противоположно действующими факторами: с одной стороны, межмолекулярным взаимодействием, обусловливающим потенциальную энергию молекул, и, с другой-тепловым движением, которое определяет их кинетическую энергию. Притяжение между молекулами, объясняющее взаимную растворимость веществ, создается за счет сил Ван-дер - Ваальса ( ориентационное, индукционное и дисперсионное взаимодействие) и водородных связей, в которых существенную роль играет донорно-акцепторное взаимодействие. [25]
Это обусловлено значительным влиянием температуры на взаимную растворимость веществ, а также тем, что допущение о применимости одного и того же интерполяционного уравнения к обоим областям гомогенных смесей, видимо, не всегда оправдывается. [26]
В этих процессах может играть существенную роль и взаимная растворимость веществ в кристаллическом состоянии. [27]
Нелинейная изотерма ( см. рис. 87 6 и 87 б) характерна для процессов, в которых проявляется сложное взаимодействие различных факторов. Это относится ко многим случаям адсорбции, а также к случаю растворения, осложненному полимеризацией, диссоциацией, взаимной растворимостью веществ, образующих две фазы, и другими явлениями. [28]
Нелинейная изотерма ( см. рис. 90, бив) характерна для процессов, в которых проявляется сложное взаимодействие различных факторов. Это относится ко многим случаям адсорбции, а также к случаю растворения, осложненному полимеризацией, диссоциацией, взаимной растворимостью веществ, образующих две фазы, и другими явлениями. [29]
Нелинейная изотерма ( см. рис. 87 6 и 87 в) характерна для процессов, в которых проявляется сложное взаимодействие различных факторов. Это относится ко многим случаям адсорбции, а также к случаю растворения, осложненному полимеризацией, диссоциацией, взаимной растворимостью веществ, образующих две фазы, и другими явлениями. [30]
Страницы: 1 2 3