Взаимная растворимость - вещество
Cтраница 3
Нелинейная изотерма ( см. рис. 90 6 и в) характерна для процессов, в которых проявляется сложное взаимодействие различных факторов. Это относится ко многим случаям адсорбции, а также к случаю растворения, осложненному полимеризацией, диссоциацией, взаимной растворимостью веществ, образующих две фазы, и другими явлениями. [31]
Известно, что процессы схватывания твердых тел происходят при взаимодействии между тонкими приповерхностными слоями, энергетические и структурные характеристики которых при любом состоянии поверхности ( ювенильная, химически адсорбировавшая атомы другого вещества или покрытая слоем оксида) существенно отличны от таковых в объеме твердого тела. В связи с большим различием в электронном строении атомов, статических и динамических параметрах решетки эти приповерхностные слои на глубине дебаевского радиуса экранирования имеют принципиально другие количественные соотношения, характеризующие способность к взаимной растворимости веществ и ее предельные ограничения. [32]
Прежде чем перейти к анализу состояния ПАВ на межфазной границе, посмотрим, что она собой представляет. На практике часто приходится иметь дело с межфазной границей, появление которой обусловлено малой растворимостью веществ друг в друге. С чем связана малая взаимная растворимость веществ, в частности воды и углеводородов. [33]
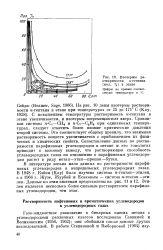 |
Изотермы растворимости н-гептана ( мол. % в этане Цифры на кривых соответствуют температуре в С. [34] |
С повышением температуры растворимость н-гептана в этане увеличивается, и изотермы перемещаются вверх. Сравнивая системы к - С7 - СН4 и к - С7 - С2Нв при одинаковых температурах, следует отметить более низкие критические давления второй системы. Это соответствует общему правилу, что взаимная растворимость веществ увеличивается с приближением их физических и химических свойств. Сопоставление данных по растворимости парафиновых углеводородов в метане и его гомологах приводит к важному выводу, что растворяющая способность углеводородных газов по отношению к парафиновым углеводородам растет в ряду метан-этан-пропан-бутан. [35]
При авто - и гетероэпитаксии кристаллический переходный эпитаксиальный слой формируется в виде областей твердых растворов на основе кристаллических решеток двух срастающихся веществ. Протяженность этого слоя определяется внешними факторами и зависит от фазовых равновесий, характерных для данной системы. Для того чтобы переходный слой имел достаточно высокую степень совершенства кристаллической структуры, необходима взаимная растворимость срастающихся веществ и определенная температура процесса, при которой еще возможно ориентированное нарастание вещества. Существенную роль играют также степень концентрационного пересыщения осаждаемого вещества, совершенство подложки И чистота ее поверхности. [36]
Растворы широко распространены в природе и имеют важное значение в химической технологии. С молекулярно-кинетической точки зрения раствор - гомогенная смесь, состоящая из нескольких веществ, находящихся в состоянии молекулярного раздробления. С точки зрения правила фаз раствором называется двух - или многокомпонентная гомогенная часть системы, состав которой может произвольно меняться в границах, определяемых взаимной растворимостью веществ. В этих определениях подчеркиваются два основных признака любого истинного раствора: его гомогенность и переменность состава. Гомогенность раствора обеспечивается равномерным распределением молекул ( или ионов) одного вещества среди молекул другого вещества. Переменность состава растворов надо понимать в том смысле, что хотя растворы образуются в результате химического взаимодействия компонентов ( Д.И. Менделеева), но в отличие от химических соединений они не подчиняются закону постоянства состава. Поэтому относительные количества веществ в растворе могут быть любыми и ограничены только их взаимной растворимостью. Растворы отличаются от химических соединений также характером и величинами энергии связи между частицами. Но возможны переходные случаи, тогда по величинам энергий связи трудно бывает отличить раствор от химического соединения. [37]
Из приведенных примеров видно, что равновесные системы можно характеризовать числом параметров или числом степеней свободы С. Эти параметры можно произвольно изменять в определенных пределах, не изменяя числа фаз. В рассмотренном случае однофазные системы характеризуются заданием двух параметров, двухфазные - одного и для трехфазных число таких параметров равно нулю. Описание фазовых равновесий в системах с большим числом компонентов ( больше одного) существенно сложнее, так как для этого требуется много данных, например о взаимной растворимости веществ. Поэтому важно установить общий закон, позволяющий найти число фаз при равновесии для систем с любым числом компонентов. Введем еще два определения, используемые в этом правиле. Фазой ( Ф) называется о д к о-родиая часть неоднородной системы, характеризующаяся определенным химическим составом и термодинамическими СЕ. Очевидно, в любой системе может быть только одна газовая фаза. Числа же твердых или жидких фаз могут быть больше. [38]
Страницы: 1 2 3