Очень высокая растворимость
Cтраница 2
Вальден 188 в своей работе обратил внимание на то, что в трихлориде мышьяка очень высокой растворимостью обладают самые различные иодиды. [16]
О том, что при растворении аммиака в воде образуется соединение, можно заключить по очень высокой растворимости и большой положительной теплоте растворения аммиа ка ( см. стр. Напротив, недиссоциированная гидроокись аммония [ NH4 ] OH в водных растворах в равновесии с ионами [ NH4 ] и ОН не существует, ибо соединение [ NH4 ] OH в недиссоциированном состоянии, как показал Бриглеб ( Briegleb, 1942), неустойчиво. Оно отличается от гидрата аммиака своим строением - это продукт присоединения. В незначительной степени, судя по уравнению ( 29а), электролитически диссоциирующий гидрат, аммиака является слабым основанием. Соответственно этому гидроокись аммония, так как она существует только в полностью диссоциированном состоянии, следует рассматривать как сильное основание. [17]
О том, что при растворении аммиака в воде образуется соединение, можно заключить но очень высокой растворимости и большой положительной теплоте растворения аммиака ( см. стр. Напротив, недиссоциированная гидроокись аммония [ NH4 ] OH в водных растворах в равновесии с ионами [ NH4 ] и ОН не существует, ибо соединение [ NH4 ] OH в недиссоциированном состоянии, как показал Вриглеб ( Briegleb, 1942), неустойчиво. Оно отличается от гидрата аммиака своим строением - это продукт присоединения. В незначительной степени, судя по уравнению ( 29а), электролитически диссоциирующий гидрат аммиака является слабым основанием. Соответственно этому гидроокись аммония, так как она существует только в полностью диссоциированном состоянии, следует рассматривать как сильное основание. [18]
О том, что при растворении аммиака в воде образуется соединение, можно заключить по очень высокой растворимости и большой положительной теплоте растворения аммиака ( см. стр. [19]
Изменение содержания свободного газа в воде, его вариации по составу и фазе обусловливают изменения в гидрохимических свойствах природных вод. Так, вследствие очень высокой растворимости углекислого газа такие факторы, как изменение минерализации, и даже относительно невысокий температурный перепад, по-видимому, повлияют на его переход в свободную фазу. Причем вследствие малых значений коэффициента диффузии всех газов в воде их обмен с атмосферой путем молекулярной диффузии, даже при наличии турбулентной конвекции на один-два порядка ниже, чем обмен через свободный газ, из-за большой скорости движения газовых пузырьков. По-видимому, при наличии микро - и макропузырьков газа их свободные границы служат источником концентрации и инициирования перехода углекислого газа в газовую фазу. По крайней мере вследствие большого числа газовых пузырьков активная поверхность межфазных границ в водных средах увеличивается на несколько порядков. Вариации углекислого газа в водной среде обусловливают и изменение таких важнейших характеристик, как рН, выделение и растворение твердой фазы. [20]
Однако вследствие того, что силы адсорбции препятствуют вымыванию ( подробнее этот вопрос будет рассмотрен ниже), оно может иметь значительные последствия только при внесении гербицидов с очень высокой растворимостью. [21]
Когда выбор возможен, то необходимо отдавать предпочтение жидкости, хорошо растворяющей поглощаемый газ, так как это свойство позволяет сократить количество циркулирующего растворителя. Иногда к очень высокой растворимости и минимальной скорости растворителя приводит обратимая химическая реакция в жидкой фазе. В таких случаях желательно иметь сведения об используемых системах; некоторые из имеющихся данных приведены на стр. Кроме того, растворитель должен быть дешевым, относительно нелетучим, стабильным, невязким. Он не должен вызывать коррозию и образовывать пену. Конечно, предпочтительны негорючие растворители. Потери растворителя с отходящим из колонны газом входят в стоимость переработки, поэтому в ряде случаев выгодно заменить дешевый растворитель более дорогим, но обладающим низкой летучестью, и высокой поглотительной способностью. Вода, применяется обычно для газов, хорошо растворимых в ней, масла - для легких углеводородов, а специальные химические растворители - для. [22]
По-видимому, разная сила действия не столь связана с растворимостью, как с другими свойствами элементов. Возможно также, что очень высокая растворимость обеспечивает большую скорость выведения яда в такой степени, что это заметно снижает его действие. [23]
Хотя алкилбензолсульфонаты применяются главным образом в виде натриевых солей, в значительном масштабе производятся магниевые и алка-ноламинные соли этих соединений. Преимущества этих солей заключаются в очень высокой растворимости в воде. [24]
Другие органические растворители менее пригодны ввиду очень высокой растворимости в них диэтилдитиофосфата никеля. Чистоту препарата достаточно контролировать по температуре плавления. Препарат удовлетворяет требованиям, предъявляемым к исходным веществам. Титрованные растворы могут быть получены растворением точных навесок в воде. [25]
Другие органические растворители менее пригодны ввиду очень высокой растворимости в них диэтилдитиофосфата никеля. [26]
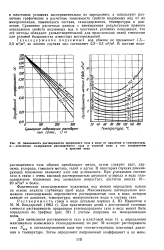 |
Зависимость растворимости природного газа в воде от давления и температуры, а - отношение содержания растворенного газа в соленой воде к его содержанию. [27] |
В некоторых случаях доминирующее положение занимают азот или углекислота. При углекислом составе газа в связи с очень высокой растворимостью двуокиси углерода в воде газосодержание подземных вод аномально возрастает, достигая иногда 10 - 20 м3 / м3 и более. [28]
 |
Растворимость в воде. [29] |
Аналогичная картина наблюдается для соответствующих азотсодержащих соединений. Алифатические амины, такие, как ди-этиламин, обладают очень высокой растворимостью в воде. Однако она увеличивается еще больше у соответствующих насыщенных гетероциклов. Сернистые аналоги здесь не рассматриваются, так как и алифатические, и циклические соединения из-за гидрофобного характера атома серы нерастворимы в воде. [30]
Страницы: 1 2 3 4