Сильно полярный растворитель
Cтраница 2
Трифенилфосфат и тиодипропионитрил как сильно полярные растворители хорошо отделяют ароматические углеводороды от алифатических углеводородов. Однако при применении трифенилфосфата не разделяются м - и и-ксилолы и этилбензол, а при применении тиодипропионитрила - м - и и-ксилолы. [16]
Наконец, в случае сильно полярного растворителя - диглицерина - эфир появляется первым, изопропиловый спирт задерживается, а кетоны выходят близко один от другого. [17]
Политиокарбаматы нерастворимы даже в сильно полярных растворителях. [18]
При применении полиамида необходимо пользоваться сильно полярными растворителями. Для полиамида рекомендуется следующий элюотропный ряд: вода - этанол - метанол - ацетон - разбавленный NaOH - формамид - диметилформамид. [19]
Vg углеводородов на умеренно и сильно полярных растворителях увеличиваются с повышением отношения количества неподвижной фазы к количеству твердого носителя. Он дает не вполне обычное объяснение этому явлению, предполагая, что с повышением этого отношения увеличивается поверхность раздела жидкость - газ и что на объем удерживания, кроме растворимости, влияет также адсорбция на этой граничной поверхности. При этом адсорбцию можно представить себе как особый случай процесса растворения, при котором растворенное вещество концентрируется в поверхностных слоях жидкости. [20]
Сефадекс набухает в воде и других сильно полярных растворителях с образованием нерастворимого геля. Объем связанного растворителя, приходящийся на 1 г сухого материала, является характеристикой степени сшивки декстрана, которая связана с проницаемостью для молекул растворенного вещества. [21]
Таким образом, ацетон относится к числу сильно полярных растворителей. Молекулы воды обладают значительной полярностью, поэтому 80 % - и 50 % - ный ацетон отличаются по полярности, причем последний более полярен. [22]
При комнатной темп-ре он растворяется лишь в сильно полярных растворителях, напр, в конц. [23]
При обычной темп-ре он растворяется лишь в сильно полярных растворителях, таких как конц. [24]
В то же время при работе в сильно полярных растворителях, например жидком SO2, катализатора не требуется. [25]
При растворении в воде, как в одном из сильно полярных растворителей, вещества претерпевают значительные изменения. В ряде случаев это проявляется в электрической проводимости водных растворов, а иногда и в полном химическом превращении растворенных веществ. Действие воды на растворенные вещества настолько сильно и специфично, что его изучение составило содержание целой области науки - химии водных растворов. [26]
Другим модельным типом растворов являются растворы ионных соединений в сильно полярных растворителях типа воды. Для переведения ионного соединения в раствор необходимо разрушить кристаллическую решетку. Растворители с высокой диэлектрической проницаемостью ( для воды е 81 7) существенно ослабляют связи в решетке и уменьшают ее энергию. [27]
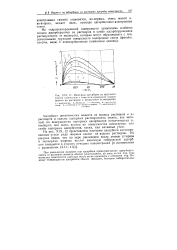 |
Изотермы адсорбции на крупнопористом силикагеле с гидроксилированной поверхностью из растворов в предельном углеводороде. [28] |
Адсорбция органических веществ из водных растворов и из растворов в сильно полярных растворителях ( таких, как метанол) на поверхностях полярных адсорбентов незначительна и, наоборот, она очень велика на поверхностях неполярных или слабо полярных адсорбентов, таких, как активные угли. [29]
В 1940 г. Траппе [202] заметил, что комбинирование высокоактивных адсорбентов с сильно полярными растворителями создает условия для химических изменений, в то время как слабые адсорбенты ( частично дезактивированный силикагель) в сочетании с растворителями низкой полярности химически неактивны. Год спустя Брокман и Шедер [203] сообщили, что разделение некоторых ПАУ улучшается при использовании частично дезактивированного оксида алюминия. Первоначально этот эффект объясняли связыванием воды наиболее активными центрами [204], что приводит к более однородной адсорбции [205], но позднее Снай-дер [206] предположил, что это является результатом удаления наиболее активных участков, что дает большее приближение к линейной изотерме адсорбции. [30]
Страницы: 1 2 3 4