Значение - константа - равновесие
Cтраница 4
Значение константы равновесия / С а) и / С В) вычислим по уравнению (82.3) при 600 К ( одна из температур, при которой проводят на производстве синтез метанола): / С. Величина / С В) примерно на 14 порядков больше, чем К а - Таким образом, при установлении равновесия в системе концентрация метанола при 600 К будет ничтожна мала по сравнению с концентрацией метана. [46]
Значения константы равновесия будут различны при разных способах ее выражения. [47]
Значение константы равновесия не зависит от того, подходит система к равновесию со стороны реагентов или со стороны продуктов. Если провести при тех же температуре и давлении любое число экспериментов с самыми разнообразными начальными концентрациями водорода, паров иода и иодово-дорода, в каждом случае будут устанавливаться не изменяющиеся со временем равновесные концентрации всех трех веществ. Эти концентрации будут отличаться от тех, что устанавливались в экспериментах 1 и 2, но вычисленная на основании новых экспериментов константа равновесия будет оставаться постоянной. [48]
 |
Зависимость In К. [49] |
Значение константы равновесия при одной температуре дает величину AG при этой же температуре. [50]
Значения констант равновесия по данным [5 ] приведены в таблице. [51]
Значение константы равновесия принято равным 1 6 - 10 - j СО и Н2 взяты в стехиометрическом соотношении. [52]
Значение константы равновесия принято равным 1 6 - 10 - Е; СО и Н2 взяты в стехиометрическом соотношении. [53]
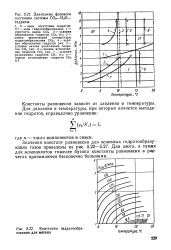 |
Диаграмма фазового состояния системы СС2 - НгО - гидраты.| Константы гидратообразования для метана. [54] |
Значения констант равновесия для основных гидратообразу-ющих газов приведены на рис. 5.22 - 5.27. Для азота, а также для компонентов тяжелее бутана константы равновесия в расчетах принимаются бесконечно большими. [55]
Значения константы равновесия приведены на рис. III. [56]
 |
Зависимость In К. [57] |
Значение константы равновесия при одной температуре дает величину AG при этой же температуре. [58]
Значение константы равновесия меняется с изменением температуры и давления. [59]
Значение константы равновесия свидетельствует о том, что реакция (13.16) должна идти слева направо практически до конца. Однако если уменьшить концентрацию ионов водорода, например, от 1 до 10 - 7 кмоль / м3, то при прочих сохранившихся условиях Дф существенно изменяется. [60]
Страницы: 1 2 3 4 5