Расчет - кривая - титрование
Cтраница 1
Расчет кривой титрования проводится совершенно аналогично предыд щему случаю. Не останавливаясь на выводе формул, который ничем существен ным не отличается от рассмотренного выше, приведем их в окончательно. [1]
Расчет кривой титрования слабого основания сильной кислотой производится вполне аналогично случаю титрования слабой кислоты. Заменяют только значения, характеристические для кислотных систем, соответствующими значениями, характеризующими основные системы. [2]
 |
Кривая титрования смеси 0 1 М молочной ( К 1 50 - Ю-4 и уксусной ( / ( 2 1 74 - ЮГ5 кислот 0 1 М раствором NaOH ( / d. / ( 2104. [3] |
Рассмотрим расчет кривой титрования смеси двух слабых одноосновных кислот HAi и НА2 разной силы ( Ка, Кд2) с одинаковой начальной концентрацией. [4]
 |
Кривая титрований О 1 М раствора аммиака 0 1 / раствором соляной кислоты. [5] |
Для расчета кривой титрования пользуются теми же формулами, что и для расчет - кривой титрования слабой кислоты, так как в титруемом растворе присутствуют те же системы: 1) до прибавления титранта раствор содержит слабое основание; 2) в процессе титрования раствор представляет собой буферный раствор; основание - - спряженная с ним кислота; 3) в точке эквивалентности в растворе содержится слабая кислота. [6]
 |
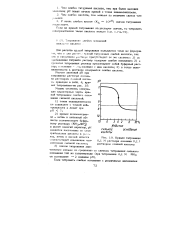
Изменение pHg при добавлении 0 05 М Hg ( NO. к 100 0 мл 0 1 М NaCl. [7] |
При расчете кривой титрования ограничимся учетом только процесса (11.1), поскольку это равновесие в условиях титрования является доминирующим. [8]
Для иллюстрации приведем расчет кривой титрования соли церия титрованным раствором сульфата железа ( 11), аналогичный сделанному авторами на стр. [9]
Основное различие в расчетах кривой титрования одно - и многоосновных кислот связано со ступенчатой диссоциацией многоосновных кислот и, как следствие, с возможным существованием двух или более скачков титрования. Кривая титрования многоосновной кислоты до первой точки эквивалентности рассчитывается по тем же соотношениям, которые использовались для расчета кривой титрования одноосновной кислоты (3.21), (3.58), учитывая диссоциацию многоосновной кислоты только по первой ступени. Возможность титрования кислоты с заданной точностью по первой точке эквивалентности зависит от соотношения ступенчатых констант диссоциации кислоты. [10]
Программу несложно переделать для расчета кривой титрования не только искусственного раствора, но и природной воды. [11]
В связи с тем что расчет кривой титрования требует некоторых затрат времени, рекомендуем Вам создать компьютерную программу расчета рН и построения кривой титрования. [12]
Рассмотренный в предыдущем разделе способ расчета кривой титрования относительно прост, но он имеет ряд недостатков. [13]
По крайней мере некоторые из этих отклонений от приближенной теории могут быть объяснены при использовании более реалистичной схемы расчета кривой титрования. Другие отклонения, видимо, связаны с особенностями конформации. Например, хорошо известно, что фенольные ОН-группы могут создавать довольно прочные водородные связи с атомами, имеющими свободные пары электронов. Энергия разрыва такой связи равна около 6000 кал / моль. Энтропия диссоциации также изменилась бы, так как можно ожидать, что образование водородных связей в белках должно ограничивать свободу вращательного движения боковых групп. Например, вращение вокруг ординарной связи между СН2 - группой и бензольным кольцом в фенольной СН2 - С6Н4 - ОН-группе должно сопровождаться вращением атома водорода гидроксильной группы вокруг оси, параллельной этой связи; если атом водорода связан водородной связью, то ясно, что такое вращение невозможно. Эти величины хорошо соответствуют аномалиям, наблюдаемым для фенольных групп сывороточного альбумина. [14]
У большинства простых многоосновных кислот константы, соответствующие отдельным ступеням диссоциации, отличаются друг от друга настолько сильно, что при расчете кривой титрования для каждой ступени можно считать, будто в каждый момент времени в растворе присутствует только одна кислота. [15]
Страницы: 1 2