Значение - коэффициент - разделение
Cтраница 1
Значения коэффициента разделения и константы равновесия совпадают лишь в случае изотопного обмена между молекулами, имеющими только по одному атому элемента, изотопный обмен которого происходит, а также для таких реакций ХИО одного атома, в которых равны произведения чисел симметрии молекул исходных веществ и продуктов реакции. [1]
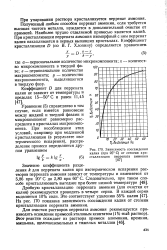 |
Зависимость соосаждения х калия ( при 25 С от степени кри. [2] |
Значение коэффициента разделения k для перрената калия при изотермическом испарении растворов перрената аммония зависит от температуры и изменяется от 5 86 при 20 С до 2 80 при 60 С. Дробную кристаллизацию перрената аммония ( для очистки от калия) рекомендуется проводить в четыре серии. В каждой серии выделяется 10 % соли. На рис. 170 показана зависимость соосаждения калия от степени кристаллизации перрената аммония. [3]
Значение коэффициента разделения в системе н - CjHie - А1 ( СНзЬС1 увеличивается от 1 5 до 3 8 с ростом концентрации н-гептана, что способствует эффективному разделению системы А1 ( СНз) гС1 - Ga ( СН3) з и решению задачи очистки выделяемого на колонне-реакторе триметилгаллия от примеси ди-метилалюминийхлорида. [4]
 |
Операторная ( а и структурная ( б схемы химического. [5] |
Значения коэффициентов разделения для любого компонента в каждом элементе ХТС определяются природой химико-технологического процесса, происходящего в элементе, параметрами элемента и зависят от параметров входных технологических потоков. [6]
Значения коэффициентов разделения разбавленных растворов винилхлорид - примесь рассчитаны по уравнениям Гилъдебранда - Скэтчарда и Мартайра. [7]
Требуется определить значения коэффициентов структурного разделения потоков и конструкционных параметров элементов ХТС, которые обеспечат минимум математического ожидания экономического КЭ функционирования ХТС при любых допустимых случайных значениях неопределенных параметров ХТП. Математическая формулировка ИЗС имеет следующий вид. [8]
Этим выражением определяется значение коэффициента разделения а для термодиффузионного метода. [9]
Необходимые для расчетов значения коэффициентов разделения галогенида и элюирующего иона были получены на основании экспериментально определенных коэффициентов распределения галогенидов. [10]
Рвыч Дает не только значение коэффициента разделения в кислой среде, но и для отдельного интервала. [11]
Для этого необходимо получить значения коэффициента разделения а бинарной смеси при трех удобных для измерений температурах. Затем строят график зависимости а от Т, вычисляют значения относительного разрешения ( R / f) и получают для этой величины кривую с максимумом, позволяющим определить оптимальные условия разделения при минимальном времени анализа. [12]
 |
Значения идеального коэффициента разцелзния в сиетеие халькогеноводород - примесь. [13] |
В табл. 4 приведены значения идеального коэффициента разделения в системе халькогеноводород - примесь. Данные таблицы показывают, что в каждом из гидридов имеются примеси, коэффициент разделения которых сравнительно близок к единице. Для сероводорода примесью, лимитирующей глубину очистки, является сероокись углерода и селеноводород, для селеново-дорода - сероводород и пропан. Вследствие этого эффективность, простой перегонки ( фракционной дистилляции) при очистке халькогеноводородов будет сравнительно невелика. Например, при простой перегонке теллуроводорода содержание селеноводо-рода ( аид 6.3) уменьшится на порядок лишь после отгонки примерно одной трети исходного гидрида. [14]
В табл. 11.7 приведены значения коэффициента разделения изотопных молекул. [15]
Страницы: 1 2 3 4