Расчет - термодинамическая функция
Cтраница 1
Расчет термодинамических функций проводится методами квантовой статистической физики. [1]
Расчет термодинамических функций химически реагирующих газов. [2]
Расчет термодинамических функций сводится к расчету суммы состояний. [3]
Расчет термодинамических функций проводится методами квантовой статистической физики. [4]
 |
Устойчивая конфигурация молекулы этана, спроектированная на плоскость, перпендикулярную оси С-С.| Зависимость потенциальной энергии от угла внутреннего вращения в этане. [5] |
Расчет термодинамических функций для дим-тилацетилена, выполненный в предположении о свободном внутреннем вращении, дает хорошее согласие с опытом. [6]
Расчет термодинамических функций доведен до 6000 К. [7]
Расчеты термодинамических функций Н2О2, выполненные Микли [2898], основаны на неправильной интерпретации колебательного спектра Н2О2, предложенной Бэйли и Гордоном [616], и поэтому ошибочны. [8]
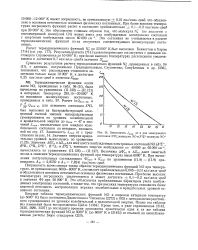 |
Зависимость Утах от v для электронного состояния Х2ПГ молекулы NO и Х1 1 молекулы N0. [9] |
Расчет термодинамических функций NJ до 25000 К был выполнен Беккеттом и Харом [714] ( см. стр. [10]
Расчеты термодинамических функций окиси и гидроокиси лития были выполнены по оцененным значениям основных частот молекул Li2O и LiOH; структурные параметры LiOH были приняты также на основании оценки. [11]
Расчеты термодинамических функций CHICHI, цис - СНТ СН1 транс - СН1СН1 транс - СД1СД1 и СЗ СЗ выполнены нами в предположении модели жесткий ротатор-гармоническйй осциллятор. [12]
Расчет термодинамических функций газов методами статистической термодинамики связан, как известно, с нахождением статистических сумм для поступательного движения и внутренних движений молекул. К числу последних относятся колебания молекул, и для расчета колебательной статистической суммы и колебательного вклада в термодинамические функции необходимо знание полного набора основных колебательных частот многоатомной молекулы в газовой фазе. [13]
Расчет термодинамических функций карбида кремния проводился для высокотемпературной гексагональной модификации, поскольку температура и теплота равновесного полиморфного превращения ( 3 - SiC в a - SiC до настоящего времени не определена. [14]
Расчеты термодинамических функций гидроокиси лития в литературе неизвестны. Значения термодинамических функций окиси и гидроокиси лития, приведенные в первом и настоящем изданиях Справочника, идентичны. [15]
Страницы: 1 2 3 4