Расчет - энтальпии - образование
Cтраница 1
Расчеты энтальпии образования ROO ( см. выше) основывали на допущении, что прочность Н - О-связи в ROOH не зависит от структуры R [7], т.е. считают, что способность передачи индуктивного влияния при замене СН2 - СН2 - группы на пероксидную труппу О-О полностью подавляется. Эти допущения дают определенную погрешность и могут быть использованы только для интерполяционных расчетов в рамках серий однотипных соединений. [1]
Для расчета энтальпии образования углеводородов рекомендуется метод Соудерса, Метьюза и Херда. [2]
Точность расчета энтальпии образования ароматических углеводородов и кислородосодержащих соединений можно существенно повысить, используя вклад Са - Н, равный - 2 66 ккал / моль. [3]
При расчете энтальпии образования полиметилзамещенных бензола в твердой фазе влияние взаимодействия метильных групп в мета - и пара-положениях оказалось мало и было принято равным нулю. Вычисленные величины энтальпии образования в твердой фазе и энтальпии сублимации алкилбензолов согласуются с экспериментальными с точностью 0 8 - 0 9 ккал / моль. [4]
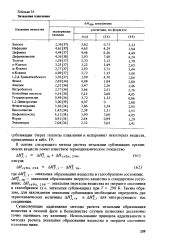
При расчете энтальпии образования по формуле (17.1) и данным табл. 17.1 необходимо учитывать следующие особенности. [5]
При расчете энтальпии образования метиладамантанов использованы вклады групп, найденные для алифатических соединений. Оказалось, что совпадение рассчитанных величин с экспериментальными хорошее, если принять напряжение адамантанового каркаса равным нулю. Такое отклонение связано, вероятно, с ошибкой эксперимента [42], так как взаимодействие гем-метильной группы с водородом СН2 - группы мало и не увеличивает напряжение молекулы, что видно из энтальпии образования 2-метиладамантана. [6]
При расчете энтальпии образования нитросоединений приняты энтальпии образования СО2 ( г) и Н2О ( ж) - 94 051 и - 68 315 ккал / моль соответственно. [7]
Предложенная схема расчета энтальпии образования позволяет с минимальным количеством исходных данных улавливать различие между АЯ / соединении с прямой и разветвленной углеродной цепью. [8]
Ключевой для расчета энтальпии образования триоксида полиоксид-ньтй вклад [ О - ( О) 2 ] не может быть рассчитан на основании имеющихся экспериментальных данных по ДЯ / и энергиям диссоциации связей родственных соединений. [9]
 |
S Энтальпия плавления. [10] |
Существующие аддитивные методы расчета энтальпии образования вещества в газовой фазе в большинстве случаев позволяют достаточно точно оценивать эту величину. Использование принципа аддитивности в методах расчета энтальпии образования вещества в твердом состоянии изложено ниже. [11]
Предложена приближенная схема расчета энтальпии образования алифатических спиртов, простых эфиров, нитратов и аминов, которая позволяет с минимальным количеством исходных данных улавливать различие между ЛЯ / соединений с прямой и разветвленной цепью. [12]
Рассмотрим для иллюстрации правила Беркенгейма расчет энтальпии образования бромида калия. Элементами-соседями брома являются хлор и иод. [13]
Следует отметить, что использованная Дузом [360] для расчета энтальпии образования газообразного CF20 величина & Нг М8 26 ккал / молъ привела к ошибочному значению ДД / 298 ( g), равному - 169 ккал / молъ. Таким образом, применение функции энергии Гиббса позволяет получить из равновесных данных такую полезную информацию, какую не могут дать достаточно надежно два первых описанных метода. [14]
МГУ, 1963 г.) указали на целесообразность расчета энтальпии образования ионных соединений через энтальпии образования ионов в бесконечно [ разбавленном растворе. [15]
Страницы: 1 2 3