Расчет - давление - насыщенный пар
Cтраница 3
Крега, Ранкина, Нернста, Риделя, Сыркина Я.К., Соколова Я.А., Филиппова Л.П., Трегубова А.Н., Киреева В.А., Тиличеева М.Д., Томсона, Мессерли и Кеннеди, Планка, Фроста-Перри, Эдмондса, Кокса, Антуана, Ашворта, Вильсона, Максвелла и др. для расчетов давлений насыщенных паров жидкостей. [31]
Крега, Ранкина, Нернста, Риделя, Сыркина Я.К., Соколова Я.А., Филиппова Л.П., Трегубова А.И., Киреева В.А., Тиличеева М.Д., Томсона, Мессерли и Кеннеди, Планка, Фроста-Перри, Эдмондса, Кокса, Антуана, Ашворта, Вильсона, Максвелла и др. для расчетов давлений насыщенных паров жидкостей. [32]
Крега, Ранкина, Нернста, Риделя, Сыркина Я.К., Соколова Я.А., Филиппова Л.П., Трегубова А.Н., Киреева В.А., Тиличеева М.Д., Томсона, Мессерли и Кеннеди, Планка, Фроста-Перри, Эдмондса, Кокса, Антуана, Ашворта, Вильсона, Максвелла и др. для расчетов давлений насыщенных паров жидкостей. [33]
Наиболее точно описывает реальный процесс модель Максвелла. Погрешность расчета давлений насыщенных паров нефти, компонентного состава газов по данной номограмме не превышает погрешности результатов хроматографического анализа. [34]
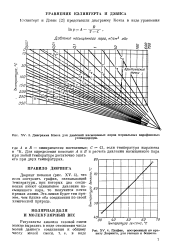 |
График, построенный по правилу Дюринга, для гексана и бензола. [35] |
А и В - эмпирические постоянные; С 43, если температура выражена в К. Для определения констант А я В к расчета давления насыщенного пара при любой температуре достаточно знать его при двух температурах. [36]
Далее необходимо определить коэффициент фугитивности насыщенного пара PHIS. Если приведенная температура TR 0 56, то для расчета давления насыщенного пара используется вириальное уравнение в форме разложения по давлению только до второго члена. [37]
В первой главе дан анализ современного состояния теории моделирования ФХС газов и жидкостей, рассмотрены известные методы их расчета. Применительно к нефтехимической технологии предложены и находят достаточно широкое применение приближенные модели ФХС, например, для расчетов давления насыщенных паров нефтяного сырья, такие формулы как Кокса, Ашворта, Максвелла и др., базирующиеся на информации только о температурах кипения фракций, что нельзя считать теоретически обоснованными. [38]
В общем случае при расчете давления насыщенных паров смесей жидкости исходят из положения, согласно которому упругость пара над всякой жидкой смесью равна сумме парциальных упругостей ее составных частей. Однако поскольку это давление зависит также и от температуры, и от соотношения в смеси компонентов и их характеристики, расчет давления насыщенного пара жидкости, состоящей из двух и более компонентов, представляет известную сложность. Она обусловлена в основном тем, что в насыщенном паре смесей жидкостей содержится большее количество легко испаряющихся ( более летучих) компонентов, чем в самой жидкости. По мере испарения жидкая фаза обедняется этими компонентами, а паровая фаза обогащается ими, причем обеднение жидкой фазы легкоиспаряющимися компонентами будет тем больше, чем больше объем парового пространства по отношению к жидкости. Вследствие этого и упругость насыщенного пара такой сложной жидкости будет тем меньше, чем выше отношение объемов паровой и жидкой фаз. [39]
Далее необходимо определить коэффициент фугитивности насыщенного пара PHIS. Для этого управление передается оператору с меткой 320, где приведенная температура сравнивается с коэффициентом, равным 0 56: Если приведенная температура TR 0 56, то для расчета давления насыщенного пара используется вириальное уравнение в форме разложения по давлению только до второго члена. [40]
Это уравнение называется уравнением Клаузиуса-Клапейрона и представляет изменение упругости пара с температурой dp / dT в зависимости от теплового эффекта процесса и удельных объемов фаз. Оно применяется для расчета давления насыщенного пара веществ или для определения их скрытой теплоты испарения. [41]
Точность результатов, получаемых при номографических расчетах, зависит, очевидно, как от масштаба номограммы, так и от точности того уравнения, по которому она построена. Последнее всегда следует иметь в виду, и применение номограмм, построенных в большом масштабе, но по недостаточно точному уравнению, не может быть ничем оправдано, так как время, затрачиваемое на расчет по ним, одинаково. К сожалению, и в наше время для расчетов давления насыщенного пара нередко применяют номограммы, построенные по менее точным уравнениям. Так, в частности, недавно была опубликована [ 377а ] сводка результатов номографического расчета давления насыщенного пара различных химических соединений, выполненная по номограмме, построенной в большом масштабе, но по уравнению вида уравнения ( 47, гл. [42]
Точность результатов, получаемых при номографических расчетах, зависит, очевидно, как от масштаба номограммы, так и от точности того уравнения, по которому она построена. Последнее всегда следует иметь в виду, и применение номограмм, построенных в большом масштабе, но по недостаточно точному уравнению, не может быть ничем оправдано, так как время, затрачиваемое на расчет по ним, одинаково. К сожалению, и в наше время для расчетов давления насыщенного пара нередко применяют номограммы, построенные по менее точным уравнениям. Так, в частности, недавно была опубликована [ 377а ] сводка результатов номографического расчета давления насыщенного пара различных химических соединений, выполненная по номограмме, построенной в большом масштабе, но по уравнению вида уравнения ( 47, гл. [43]
Следует отметить, что при использовании уравнения (4.13) и равенства (4.30) значение коэффициента А должно быть равным для любых веществ. Это следует из условий (4.7), характеризующих критическую точку. Однако авторы [1,2] для углеводородов от н-гексана до н-декана, для азота, диоксида углерода и сероводорода получили различные значения коэффициента А. Фундаментальные условия (4.7) не были использованы, а значение коэффициента А определялось из уравнений (4.13), (4.30) после подстановки Т Тс р рс, и ис. Такой подход означает лишь то, что коэффициент А определяется по одной точке, для которой известны экспериментальные значения давления, температуры и мольного объема. При этом для уравнения состояния нет никаких признаков о том, что эта точка - критическая. В свою очередь, неверное определение критической точки приводит к погрешностям при расчете давления насыщенного пара вещества, области существования жидкой фазы. Это отрицательно влияет и на точность расчета парожидкостного равновесия смесей веществ. [44]
Страницы: 1 2 3