Стехиометрический расчет
Cтраница 3
Расчеты по химическим уравнениям ( стехиометрические расчеты) основаны на законе сохранения массы веществ. Однако в реальных химических процессах из-за неполного протекания реакции и различных потерь веществ масса образующихся продуктов часто бывает меньше той, которая должна образоваться в соответствии с законом сохранения массы веществ. [31]
Количественное соотношение реагентов определяется не только стехиометрическим расчетом ( по анализам сырья с учетом потерь), но и заданным литражом карбида кальция. С увеличением количества углерода в шихте литраж карбида повышается, хотя выход его при этом уменьшается. При высоком содержании в шихте извести выход карбида увеличивается, одновременно уменьшается его литраж. Согласно опытным данным, наибольший выход высоколитражного карбида кальция получается при содержании в шихте 55 - 60 % углерода; наивысшее же качество карбида ( литраж) достигается при содержании в шихте 72 % углерода. В заводских условиях обычно применяют шихту, содержащую 40 - 50 % С. [32]
Из уравнения ( 21) с помощью элементарных стехиометрических расчетов можно легко вычислить значения теплотехнических показателей процесса горения углерода. Результаты расчетов показывают, что в зависимости от степени превращения двуокиси углерода теплотехнические показатели процесса горения углерода изменяются в довольно широких пределах. [33]
Непосредственного способа использования летучей части твердого вещества для стехиометрических расчетов нет, но безусловно, можно измерить как ХПК, так и летучую часть твердого вещества в сточных водах и при наличии некоторого опыта составить полезное соотношение между этими двумя параметрами. Значения, приводимые в табл. 6.7.1, основаны на опытных данных. Твердое вещество, поступающее в анаэробный реактор, солюбилизи-руется и ферментируется вместе с другими веществами. Темпы роста анаэробных организмов, обеспечивающих ферментацию настолько малы, что мы можем измерить чистые потери твердого вещества. [34]
В крупнотоннажном производстве количество сероуглерода превышает необходимое по стехиометрическому расчету. Избыток сероуглерода при неплотности аппаратуры может выделяться в цех. Следует иметь в виду, что весь процесс ксантогениро-вания является взрывоопасным; кроме того, сероуглерод - сильнодействующий яд. Поэтому персонал завода, особенно ксантатного цеха, должен хорошо знать свойства сероуглерода и строго выполнять правила техники безопасности. [35]
Поэтому потребное количество извести лишь предварительно определяется по стехиометрическому расчету исходя из загрязненности обрабатываемой воды, по концентрации активной СаО в известковом молоке и по заданному рН воды, которое необходимо для протекания всех реакций. [36]
Поэтому потребное количество извести лишь предварительно определяется по стехиометрическому расчету исходя из загрязненности обрабатываемой воды, по концентрации активной СаО в известковом молоке и по заданному рН ВОДЫ, которое необходимо для протекания всех реакций. [37]
Выход реакции обычно значительно ниже теоретического ( найденного стехиометрическим расчетом) по следующим причинам: 1) обычно перед достижением состояния равновесия реакция получения целевого продукта прерывается ( разность скоростей прямой и обратной реакций очень мала); 2) главной реакции часто сопутствуют побочные, приводящие к увеличению расхода исходных веществ; 3) в технологическом процессе существуют различные потери, не учтенные в теоретическом расчете. [38]
Приведенные ниже примеры иллюстрируют применение треугольных фазовых диаграмм для простых стехиометрических расчетов. [39]
Введением в анализ химической концепции является установление с помощью стехиометрических расчетов количеств основных и вспомогательных веществ, которые теоретически необходимы для получения определенного количества продукта. Расчеты основаны на законах сохранения массы, постоянства состава и кратных отношений, а также на законе действия масс, если реакция обратима и известно значение константы равновесия. [40]
 |
Технологическая схема установки для очистки сточных вод от хрома с применением ABC. [41] |
Расход Са ( ОН) г по отношению к стехиометрическому расчету составляет 100 % Наличие Сг3 после нейтрализации не обнаружено. [42]
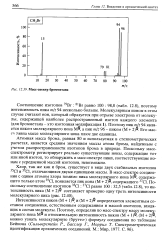 |
Масс-спектр бромметана. [43] |
Атомная масса брома, равная 80 и используемая в стехиометрических расчетах, является средним значением массы атома брома, найденным с учетом распространенности изотопов брома в природе. Поскольку масс-спектрометр регистрирует реально существующие ионы, содержащие тот или иной изотоп, то обнаружить в масс-спектре пики, соответствующие ионам с усредненной массой изотопов, невозможно. [44]
Так как конечным продуктом восстановления являются ионы брома, то стехиометрические расчеты ведут, пользуясь уравнением для бромат-ионов. [45]
Страницы: 1 2 3 4