Малое расщепление
Cтраница 1
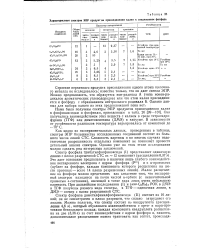 |
Характеристики спектров ЭПР продуктов присоединения калия к соединениям фосфора. [1] |
Малое расщепление на фосфоре можно представить как следствие того, что неспаренный электрон находится на почти чистой а-орбите ( с незначительной примесью s - состояния), имеющей в точке ядра лишь очень небольшую плотность. При дальнейшем исследовании ( I) и ( изо - С3Н7) з РОК в ДМЭ и ТГФ получены разного вида спектры, в ТГФ - одиночная линия, в ДМЭ - спектр с плохо разрешенной СТС. [2]
Малое расщепление линий, достигающее для этой ориентации максимальной величины 10 гс, обусловлено сверхтонким взаимодействием лишнего электрона в XeF с ядром фтора соседней молекулы XeF4, - так называемое, взаимодействие ближних соседей. [3]
Оно характеризует относительно малое расщепление энергетического уровня, определяемого квантовым числом L, на 25 1 ( или 2L 1) близких уровней, называемое мультиплетным расщеплением. Поэтому электронное состояние атома помимо электронной конфигурации определяют значениями квантовых чисел L и 5 и соответствующий ему уровень энергии называют термом. [4]
Сигналы метиновых групп представляют собой триплет с очень малым расщеплением, связанным с резонансами протонов метиленовых групп. Наибольшая чувствительность к конфигурации характерна для резонансов нитрильной группы, где наблюдается почти идеальное распределение Бернулли. Резонансные сигналы метиновых групп в полиакрилонитриле располагаются в порядке rr, mr и mm от низких полей к высоким. [5]
Поэтому здесь возможно изучение таких взаимодействий в веществе, к-рые вызывают очень малые расщепления энергетич. [6]
Для несимметричного соединения этот спектр практически наблюдается в виде дублета с малым расщеплением, так как внешние пики квадруплета имеют малую интенсивность. В симметричном соединении химический сдвиг 8АВ несколько больше, и наблюдаются все четыре линии системы ABf В tyuc - соединениях химический сдвиг примерно в десять раз больше, а величина JAB вдвое меньше, поэтому интенсивности компонент соответствующего спектра близки. [7]
Лиганды, расположенные в конце спсктрохимнче-ского ряда ( лиганды слабого поля), вызывают малое расщепление энергии rf - подуровня. В этом случае энергия взаимного отталкивания двух спаренных электронов оказывается более высокой, чем энергия расщепления. Поэтому rf - орбитали заполняются электронами в соответствии с правилом Хунда: первые три электрона распределяются по одному на с / Е - орби-талях, а следующие два - на dy - орбиталях. Только после этого начинается попарное заполнение электронами сначала de -, а затем dy - орбиталей. [8]
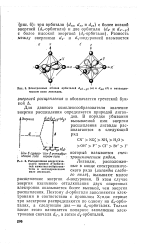 |
Электронные облака орбиталей Лхч-уг ( а и dxa ( б в октаэдри-ческом поле лнгандов. [9] |
Лиганды, расположенные в конце спектрохимиче-ского ряда ( лиганды слабого поля), вызывают малое расщепление энергии - подуровня. В этом случае энергия взаимного отталкивания двух спаренных электронов оказывается более высокой, чем энергия расщепления. Поэтому cf - орбитали заполняются электронами в соответствии с правилом Хунда: первые три электрона распределяются по одному на с. Только после этого начинается попарное заполнение электронами сначала dE -, а затем а у-орбиталей. [10]
Лиганды, расположенные в конце спектрохимиче-ского ряда ( лиганды слабого поля), вызывают малое расщепление энергии d - подуровня. В этом случае энергия взаимного отталкивания двух спаренных электронов оказывается более высокой, чем энергия расщепления. Поэтому d - орбитали заполняются электронами в соответствии с правилом Хунда: первые три электрона распределяются по одному на de - орбита-лях, а следующие два - на dy - орбиталях. Только после этого начинается попарное заполнение электронами сначала de -, а затем dy - орбиталей. [11]
 |
Расщепление энергетического уровня d - орби-талей комплексообраэо-вателя воктаэдрическои поле лигандов. [12] |
Лиганды, расположенные в конце спектрохимического ряда ( лигандщ слабого поля), вызывают малое расщепление энергии й-подуровня. В этом случае энергия взаимного отталкивания двух спаренных электронов оказывается более высокой, чем энергия расщепления. Поэтому rf - орбитали заполняются электронами в соответствии с правилом Хунда: первые три электрона распределяются по одному на с - орбиталях, а следующие два - на dy - орбиталях. Только после этого начинается попарное заполнение электронами сначала da -, а затем dy - орби-талей. [13]
Правильное было бы учитывать штарковскую структуру мулычшлета 3Л2, но в связи с его малым расщеплением ( - 6 с. [14]
В невырожденных состояниях очень слабое магнитное поле появляется в результате вращения молекулы, и это обусловливает очень малое расщепление на 25 1 компонент. [15]
Страницы: 1 2 3