Триплетное расщепление
Cтраница 2
Эти измерения показали, что дифенилкарбен, фе-нилкарбени флуоренилиден имеют триплетное основное состояние. Величина триплетного расщепления в нулевом поле и сверхтонкие расщепления на протонах показывают, что в случае дифе-нилкарбена обе фенильные группы расположены приблизительно, но не точно перпендикулярно друг другу. [16]
Спектр протонов молекулы ( рис. 1 - 10, а) состоит, из 6 линий, образующих два триплета. Очевидно, что триплетное расщепление вызвано наличием двух атомов фтора, так что константу / HF можно определить, измерив расстояния между соседними компонентами в триплетах и взяв среднюю величину. Присутствие одного атома фосфора вызывает дублетное расщепление протонов, причем константу / нр можно, очевидно, получить, измерив расстояния между соответствующими компонентами, принадлежащими двум различным триплетам, например между центральными пиками этих триплетов. Для получения более точного результата полезно взять среднее из трех возможных измерений. Кроме того, из спектра протонного резонанса можно определить химический сдвиг протонов, измерив расстояние от центра сигнала метильной группы до сигнала эталона. Все измерения производятся по вершинам пиков. [17]
Спектры атомов цинка, кадмия и ртути сходны между собой. Зависимость энергии от квантового числа / при данных L и S определяет значение триплетного расщепления: для больших атомных номеров расщепление имеет большее значение. [18]
Действительно, анализ вращательной структуры первой системы согласуется с предположением о том, что верхнее состояние системы представляет собой состояние типа1 - Однако Дуглас [293] показал, что в рассматриваемых полосах CS2 наблюдается заметное зеемановское расщепление, свидетельствующее о наличии в возбужденном состоянии магнитного момента, что позволяет в свою очередь сделать вывод о том, что возбужденное состояние должно быть триплетным. Следует тем не менее отметить, что ни в одной из исследованных полос поглощения триплетное расщепление не было найдено. [19]
Позднее в другой работе были приведены значения частот всех трех колебаний для молекул А120, Ga20, In20 и Т120, которым на основании положения полос мг и v2 была приписана структура с очень небольшим острым углом MOM и значительным взаимодействием между атомами металла. Дальнейшие исследования показали ошибочность этого вывода: частичное изотопное замещение ( 180) приводит к триплетному расщеплению полос ( неправильно отнесенных к колебаниям Vj и v2 молекул Ga20 и 1п20) и, следовательно, указывает на их соответствие молекулам с двумя атомами кислорода. [20]
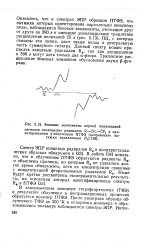 |
Боковые компоненты первой производной. [21] |
ПЦ, с которым связаны эти линии, дают также вклад в центральную часть суммарного спектра. Данный спектр можно приписать концевым радикалам R9, так как расщепление в 390 э могут дать только два а-фтора. Триплетное расщепление боковых компонент обусловлено двумя 3-фто-рами. [22]
Структура первой из трех подполос очень похожа на структуру полосы 0 - О, за исключением того, что все линии в ветвях удвоены из-за / - удвоения в нижнем состоянии. Для NCN или ССО было разрешено лишь очень небольшое число из всех 54 ветвей. В двух других под-полосах наблюдается триплетное расщепление, которое быстро увеличивается с ростом N. Первые из этих подполос связаны с верхними состояниями 3Е i, а вторые - с состояниями 32э - и 32з соответственно. [23]
Для масс-спектров, как правило, характерно наличие интенсивного пика мол. Интенсивность пиков ионов [ М 1 ] превышает интенсивность пика изотопного иона. В спектрах ЭПР Н.р. проявляется триплетное расщепление, обусловленное сверхтонким взаимод. [24]
В красной ( синглетной) системе полос ( фиг. Следует отметить, что, хотя триплетное расщепление в системе 32U - 32g до настоящего времени не разрешено, имеются косвенные, весьма убедительные данные, свидетельствующие о триплетном характере рассматриваемого перехода. [25]
Интересной особенностью полос HSiCl и HSiBr является присутствие в спектре помимо ветвей с & К 1 и 0, ветвей с &. Появление этих полос не может быть объяснено отклонением структуры молекулы от симметричного волчка, так как эти отклонения пренебрежимо малы ( 6 - 0 00052 для HSiCl), и даже в спектрах значительно более асимметричных молекул не имеется никаких намеков на такие ветви, которые в согласии с теорией должны иметь очень малую интенсивность. Герцберг и Верма [545] и Хоуген [574] высказали предположение, что причиной подобной аномалии является спин-орбитальное взаимодействие, или, другими словами, что наблюдаемый электронный переход является переходом типа 3А - 1Л ( см. стр. Однако отсутствие заметного триплетного расщепления ставит под сомнение такую интерпретацию. В качестве альтернативы можно, очевидно, рассматривать преобразование ( поворот) осей ( см. стр. [26]
Установлено [124], что молекулы типа 1гК ( циклооктадиен) Ьг, где R CH3 или Н, L Р ( С6Н5) ( СН3) 2, Р ( С6Н5) 2 ( СН3) или Р ( С6Н5) з, стереохимически лабильны. В предельном низкотемпературном спектре ЯМР каждого соединения наблюдаются два ви-нильных и два широких метиленовых сигнала от циклооктадиена, а сигнал от R расщепляется на триплет, что свидетельствует об одинаковом взаимодействии с обоими ядрами фосфора. Диасте-реотопные метальные группы лиганда Р ( С6Н5) ( СН3) 2 приводят к появлению двух мультиплетов. При предельной скорости обмена уравнивания резонансов двух диастереотопных метальных групп не происходит; сохраняется и триплетное расщепление сигнала от R. Эти результаты согласуются с механизмом Берри. [27]
Спектр диметилфенилфосфинкалия состоит из - 24 линий СТС. Дублет следует связать с расщеплением на фосфоре, квадруплет - с взаимодействием с орто - и пара-протонами бензольного кольца, септет - с шестью протонами метальных групп. Впрочем, нельзя отбросить и предположение о взаимодействии с мета-протонами, которое должно дать не септетное, а триплетное расщепление; в этом случае следует предположить, что две слабые линии на краю спектра не относятся к обсуждаемому радикалу. Характер ориентации фосфиногруппы при замещениях в бензольном кольце неизвестен. Однако известно, что в непредельных фосфинах типа CH2 CHPR2 имеет место р-ориентация нуклеофильных реагентов [97], что согласуется с отнесением группы PR2 к ориентантам второго рода. [28]
Они характеризуются наличием одиночных и триплетных серий, относительно глубоким расположением нормального уровня ns21S0 и наличием метастабильных уровней tts np 3Р0 и nsnp P. У всех этих элементов наблюдаются интеркомбинационные переходы между одиночными и триплетными уровнями, причем чем тяжелее элемент, тем более вероятны эти интеркомбинационные переходы. На рис. 83 приведены схема уровней и возникновение основных линий в спектре Cal. На рис. 84 дано расположение термов Bel, Mgl, Znl, Cd I и HgI ( без учета триплетного расщепления) в сравнении с термами водорода. [29]
До сих пор не наблюдалось ни одного дублет-квартетного перехода 1), однако примеров синглет-триплетных переходов известно много ( гл. Наблюдавшуюся фосфоресценцию большого числа сложных многоатомных молекул Льюис с сотрудниками объясняют переходами из первого возбужденного ( триплетного) электронного состояния в основное ( синглетное) состояние. Вполне ясным представляется переход 3AZ - А в молекуле формальдегида ( Ди Джорджио и Робинсон [278], Райнес [1060]), интеркомбинационная природа которого была установлена наблюдением триплетного расщепления. Так же как в атомах и двухатомных молекулах, триплет-синглетный переход становится в этом случае возможным из-за смешивания триплетного и синглетного состояний. Синглетное же состояние интенсивно комбинирует с основным состоянием. [30]
Страницы: 1 2