Электролитическое рафинирование - алюминий
Cтраница 1
Электролитическое рафинирование алюминия является одним из наиболее энергоемких процессов в металлургии легких металлов, причем 93 - 95 % используемой энергии расходуется на поддержание теплового режима электролизера. Независимо от мощности электролизеров 65 - 75 % потерь тепла происходит через верх электролизера, а падение напряжения в электролите составляет 80 - 85 % в общем балансе омического падения напряжения на электролизере. Следовательно, основными определяющими факторами удельного расхода электроэнергии являются высота слоя электролита ( падение напряжения в электролите пропорционально высоте его слоя) и теплоизоляция верха электролизера. [1]
 |
Ванна для рафинирования алюминия. [2] |
Электролитическое рафинирование алюминия, как и тяжелых металлов, основывается на том, что из анода, состоящего из загрязненного металла, переводят в раствор только алюминий и более отрицательные металлы, на катоде же из раствора выделяется только алюминий. [3]
Метод электролитического рафинирования алюминия называют трехслойным: анод расположен на дне ванны, на его поверхности находится электролит, а сверху плавает катод. Анод и катод включены в электрическую цепь графитовыми стержнями. [4]
При электролитическом рафинировании алюминия галлий, обладая менее электроотрицательным потенциалом, чем первый, накапливается в анодном сплаве, откуда может быть извлечен. [5]
При электролитическом рафинировании алюминия более электроположительные примеси железа, кремния, меди и др. остаются в анодном сплаве. [6]
 |
Структура себестоимости алюминия. [7] |
На чем основан метод электролитического рафинирования алюминия. [8]
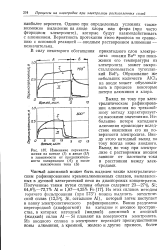 |
Изменение перенапряжения на катоде ( / и аноде ( / / в зависимости от продолжительности поляризации ( А и после выключения тока (. [9] |
Выход по току при электролитическом рафинировании алюминия по трехслойному методу характеризуется высокими значениями. Небольшие потери катодного алюминия происходят вследствие окисления его на поверхности электролита. [10]
Известны двухслойный и трехслойный методы электролитического рафинирования алюминия. [11]
Типичным процессом электролиза расплавленных солей с растворимым анодом является электролитическое рафинирование алюминия, заключающееся в анодном растворении алюминия ( из сплава с другими металлами) с переходом ионов Als в электролит и в разряде этих ионов на катоде. При электролитическом рафинировании алюминия жидкий анодный сплав состоит из алюминия и меди и небольших примесей других элементов. Элементы, более электроположительные, чем алюминий ( медь, железо, кремний и др.), присутствующие в анодном сплаве, не подвергаются анодному растворению и накапливанию до определенной концентрации в жидком анодном сплаве, тогда как металлы с более электроотрицательным потенциалом, чем у алюминия ( натрий, кальций, магний и др.), переходят в электролит. [12]
В ряде случаев применяют графитированные электроды, например в качестве катодов в электролизерах для электролитического рафинирования алюминия. Такие электроды получают из угольных электродов путем их нагрева до температуры порядка 2500 С. При нагреве до такой температуры так называемый аморфный углерод превращается в кристаллический графит. Присутствующие в электроде минеральные примеси образуют карбиды, которые при высокой температуре диссоциируют, при этом кремний, железо и другие металлы удаляются в парообразном состоянии. [13]
Типичным процессом электролиза расплавленных солей с растворимым анодом является электролитическое рафинирование алюминия, заключающееся в анодном растворении алюминия ( из сплава с другими металлами) с переходом ионов Als в электролит и в разряде этих ионов на катоде. При электролитическом рафинировании алюминия жидкий анодный сплав состоит из алюминия и меди и небольших примесей других элементов. Элементы, более электроположительные, чем алюминий ( медь, железо, кремний и др.), присутствующие в анодном сплаве, не подвергаются анодному растворению и накапливанию до определенной концентрации в жидком анодном сплаве, тогда как металлы с более электроотрицательным потенциалом, чем у алюминия ( натрий, кальций, магний и др.), переходят в электролит. [14]
Рафинирование алюминия трехслойным способом сходно с электролитическим рафинированием меди и отличается от него тем, что протекает не в водном растворе, а в расплавленных солях и не с твердыми, а с жидкими электродами. Перенос тока при электролитическом рафинировании алюминия сводится к образованию у анода ионов алюминия, которые, направляясь к катоду, выделяются в виде металлического алюминия. [15]
Страницы: 1 2