Элек-трофильный реагент
Cтраница 2
Таким образом, реакционная способность перфторолефинов в данном случае находится в соответствии с другими примерами свободно радикального присоединения элек-трофильных реагентов. [16]
Эффективные л-электронные заряды показывают, что в о - и п-положеннях имеется недостаток электронов, что делает атаку элек-трофильного реагента в этих положениях маловероятной. [17]
В свою очередь реагенты, образующие новую связь за счет электронной пары реагирующего с ним вещества, называются элек-трофильными реагентами. [18]
Таким образом, с некоторым приближением можно сказать, что в случае ароматических радикалов, чем легче радикал отщепляется элек-трофильными реагентами, тем труднее он отщепляется нуклеофильными реагентами. [19]
Как мы видели, стерические препятствия могут подавить активирующее влияние нитрогруппы по отношению к нуклеофильным реагентам, а в случае элек-трофильных реагентов возможно, что будет подавлено влияние аминогруппы. Это следует из того факта, что структуры класса В, вроде структуры XIII для реакции анилина с бромом, наиболее стабильны, если два атома водорода аминогруппы лежат в плоскости бензольного кольца. [20]
Хорошо известно, что некоторые группы заместителей, расположенные около реакционного центра, посредством резонанса могут отдавать этому центру электроны или увеличивать на нем электронную плотность посредством индуцирования, поэтому реакции с нуклеофильными реагентами на таком центре протекают медленнее, а с элек-трофильными реагентами быстрее. Наоборот, если эти группы оттягивают электроны от реакционного центра, реакция с нуклеофильными реагентами должна протекать быстрее, чем с электрофильными. [21]
Циклобутадиеновый ли-ганд в комплексе C4H4Fe ( CO) 3 имеет ароматический характер в том смысле, что он вступает в реакции электрофильного замещения, давая новые замещенные циклобутадисновые комплексы. По-видимому, реакционная способность циклобутадиснового ли-ганда в отношении элек-трофильных реагентов сравнима с реакционной способностью ферроцена. [22]
Это этиленовое соединение было получено в виде двух цис-транс-изомеров. В этих изомерах остаток HgCl может быть замещен элек-трофильными реагентами, причем органический радикал сохраняет свою стерическую конфигурацию. [23]
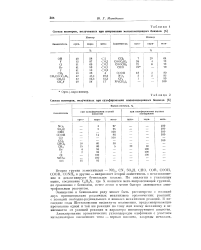 |
Состав изомеров, полученных при нитровании монозамещенных бензола. [24] |
Вторая группа заместителей - N02, CN, S03H, СНО, COR, COOH, GOOR, CONH2 и другие - направляет второй заместитель и мета-положение и дезактивирует бензольное кольцо. По аналогии с указанным выше, соединение СвНБХ, где X является мета-направляющей группой, по сравнению с бензолом, менее легко и менее быстро замещается элек-трофильным реагентом. [25]
В настоящее время диоксид хлора является наиболее мягким и избирательным хлорсодержащим реагентом. Химизм реакций делигнификации и отбелки диоксидом хлора полностью не изучен. Диоксид хлора - элек-трофильный реагент, который быстро реагирует со структурами, содержащими свободный фенольный гидроксил и медленно - с насыщенными алифатическими соединениями. В связи с этим воздействие СЮг на целлюлозу, окисленную ранее, например, после кислородно-щелочной делигнификации, менее эффективно. [26]
Для вычисления энергии локализации вычисляют энергию двух структур: исходной и переходной. Так, например, желая вычислить энергию локализации на определенном атоме в молекуле бензола при атаке нуклеофильным реагентом, находят энергию шести я-электронов в остове, состоящем из пяти атомов углерода ( переходная структура), и вычитают эту энергию из энергии бензола; при этом выключается именно тот атом, на котором надо определить энергию локализации. Если атака производится элек-трофильным реагентом, стремящимся присоединиться к более отрицательному атому бензола, то надо найти энергию четырех электронов, распределенных между пятью атомами углерода, и энергию двух электронов у изолированного атома и затем вычесть сумму этих величин из энергии бензола. [27]
 |
Уровни энергии, значелия - 2. энергии МО л-электропной системы молекулы бутадиена-1 3 й.| Очертания МО молекулы бутадиена-1 3 2 / 3. [28] |
ВЗМО и НСМО называются фронтальными орбиталями; они определяют реакционную способность сопряженной системы. Энергия ВЗМО по абсолютному значению соответствует энергии ионизации орбнтали и определяет элект-ронодонориые свойства, взаимодействие с электрофильпыми реагентами. Распределение плотности электронов в орбнтали обусловливает места атаки элек-трофильных реагентов. [29]
Одной из наиболее часто применяемых нуклеофильных реакций нитрильной группы является реакция Риттера, которая проводится в присутствии серной кислоты и других протонных кислот и приводит к образованию новой связи N-С. Большое теоретическое и практическое значение имеют реакции нитрилов в присутствии апротонных кислот, в результате которых образуются нитри-лиевые соли и продукты их превращения. В данной главе рассмотрены также реакции нитрилов с хлорангидридами карбоновых кислот, которые осуществляются в присутствии апротонных кислот или без применения каких-либо катализаторов, нуклеофильные реакции нитрилов с различными трехчленными циклами, завершающиеся расширением циклов или получением соединений линейного строения, оригинальные стереоспецифические реакции одновременного воздействия на олефины нитрилов ( играющих в данном случае роль нуклеофильных соединений) и некоторых элек-трофильных реагентов. Завершается глава описанием ряда малоизвестных или недостаточно исследованных реакций нитрилов, приводящих к образованию новой связи N-С. [30]
Страницы: 1 2 3