Изученный реагент
Cтраница 1
Изученные реагенты можно разделить на четыре группы: реагенты на основе о-аминофениларсоновой, антраниловой, пикрами-новой кислот и аминосульфохлорфенола. [1]
Наиболее изученными реагентами этого типа являются диэтилдитиофосфорная и дибутилдитиофосфорная кислоты. [2]
Наиболее изученными реагентами этого типа являются ди-н-бутил - и ди-2 - этилгексилфосфорная кислоты. [3]
Наиболее изученным реагентом рассматриваемого класса соединений является салицилаль-о-аминофенол. Введение различных заместителей как в аминную, так и альдегидную часть молекулы не дает значительного аналитического выигрыша при применении этих реагентов. В то же время переход к бис-производным позволяет резко увеличить чувствительность определения ряда элементов и упростить условия их аналитического использования. [4]
Другим хорошо изученным реагентом радикального галогенирования ярляется трет-бутилгипохлорит. [5]
В целях применения изученного реагента в аналитической практике нами была исследована зависимость интенсивности окраски экстрактов от концентрации соответствующего катиона, В связи с тем, что светопоглощение соединений меди и ванадия с ДБО максимально при 420 и 410 нм соответственно, оптическую плотность при построении калибровочных графиков для каждого элемента измеряли на указанной длине волны. Экспериментальные данные были обсчитаны по методу наименьших квадратов. Как показывают расчеты [22], градуировочный график для ванадия при рН 2 описывается уравнением у 0 39х, для меди при том же рН - уравнением у 0 0& г при рН 10 - уравнением у O. ILr, где у-оптическая плотность растворов, а: - концентрация определяемого металла. [6]
Ксиленоловый оранжевый [7] является наиболее хорошо изученным реагентом этой группы и применяется для определения ниобия [8-10], циркония [11-13], суммы [14] и индивидуальных редкоземельных элементов [15, 16], скандия [17], индия [18], урана, тория, висмута, железа, алюминия, молибдена, фтора и других элементов. [7]
Ксиленоловый оранжевый [7] является наиболее хорошо изученным реагентом этой группы и применяется для определения ниобия [8-10], циркония [ И-13 ], суммы [14] и индивидуальных редкоземельных элементов [15, 16], скандия [ 171, индия [18], урана, тория, висмута, железа, алюминия, молибдена, фтора и других элементов. [8]
Действительно, сравнение констант кислотной диссоциации изученных реагентов ( гГ) т 2 20 - 10-пи HjBm 3 28 - Ю-10) показывает, что бензоилметилдиоксим обладает более ясно выраженными кислотными свойствами, или, иными словами, водород оксимной группы последнего более подвижен, чем водород оксимной группы диметилдиоксима. Сравнительно небольшое различие констант кислотной диссоциации упомянутых реагентов объясняется относительно слабым отрицатель - ным индукционным эффектом группы СвН6 - и некоторой удаленностью последней от оксимной группы. [9]
Контрастные цветные реакции при взаимодействии с изученными реагентами дает также медь. [10]
В заключение следует отметить, что все изученные реагенты относятся к 3 - 4-му классам токсичности и опасности. Это определяет соответствующий объем требований соблюдения правил техники безопасности, осуществления необходимых мер коллективной и индивидуальной защиты работающих. Произведенные расчеты показали, что по классификации степени опасности веществ в воде водных объектов, рассмотренные нами химические реагенты относятся к 3 - 4-му классам. В соответствии с методической схемой этапного обоснования гигиенических ПДК химических веществ в воде водных объектов, в данном случае применима схема ускоренного нормирования реагентов по результатам изучения влияния их на органолептические свойства воды, общий санитарный режим водоемов, данных острого и по-дострого опытов и расчета ЛШД. [11]
На основании сопоставления пороговых величин по трем показателям вредности для всех изученных реагентов лимитирующим является органолептический признак. [12]
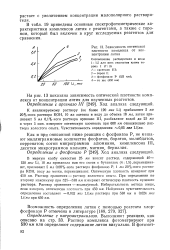 |
Зависимость оптической плотности комплекса от концентрации лития. [13] |
На рис. 13 показана зависимость оптической плотности комплекса от концентрации лития для изученных реагентов. [14]
Несмотря на сравнительно небольшую чувствительность, которую различные авторы оценивают по-разному, тиомочевина остается одним из наиболее употребительных и хорошо изученных реагентов для спектрофотометрического определения осмия. В связи с этим следует напомнить, что недостаточную чувствительность реагента можно вполне компенсировать легкостью концентрирования осмия, если его предварительно отогнать или проэкстрагировать. [15]
Страницы: 1 2 3