Димагнийфосфат
Cтраница 2
 |
Изотермы растворимости в системе MgO - РгО6 - Н2О при 25, 80 и 130 С. [16] |
Как и для солей кальция, с увеличением концентрации Р2О5 растворимость димагнийфосфата растет, а мономагнийфос-фата уменьшается ( см. рис. 4.14), но в отличие от монокальций-фосфата степень разложения водой мономагнийфосфата почти не зависит от температуры. [17]
Как и для солей кальция, с увеличением концентрации Р2О5 растворимость димагнийфосфата растет, а мономагнийфосфата - уменьшается ( см. рис. 71), но в отличие от монокальцийфосфат степень разложения водой мономагний-фосфата почти не зависит от температуры. [18]
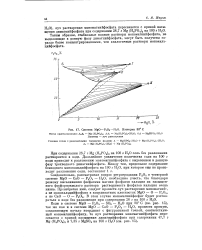 |
Система MgO - Р305 - Н20. Изотерма 80 С. [19] |
Таким образом, стабильные водные растворы мономагнийфосфата, не выделяющие в донную фазу димагнийфосфата, могут быть получены гораздо более концентрированными, чем аналогичные растворы монокальцийфосфата. [20]
Так же как и при 25, в изученной области концентраций растворы, насыщенные димагнийфосфатом, инконгруэнтны по отношению к последнему. То же относится и к растворам, насыщенным двуводным и безводным мономагнийфосфатом. [21]
В присутствии солей магния ( например, в фосфоритах Каратау) по аналогичным реакциям образуется димагнийфосфат. Такая глубокая аммонизация приводит к ретроградации водорастворимой формы P2Os, но содержание усвояемой P2Os при этом уменьшается незначительно. [22]
В более старых работах, посвященных исследованию фосфатов магния ( см. [5]), упоминаются для димагнийфосфата гепта -, три - и моногидрат, а для мономагнийфосфата - дигидрат и безводная соль. [23]
При титровании смесей Н РО4 и Mg ( H2PO4) 2 вычисленное содержание мономагнийфосфата, в предположении образования димагнийфосфата, хорошо совпадало с действительным содержанием его в контрольной смеси. [24]
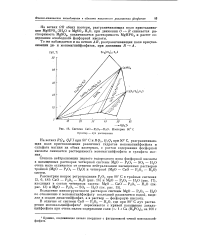 |
Система СаО - Р206 - Н20. Изотерма 80 С. [25] |
Вследствие инконгруэнтности растворов системы MgO - Р205 - Н20 по отношению к мономагнийфосфату последний разлагается водой, выделяя в осадок димагнийфосфат, а в раствор - фосфорную кислоту. [26]
Вследствие инконгруэнтности растворов системы MgO - Р2О5 - Н2О по отношению к мономагнийфосфату последний разлагается водой, выделяя в осадок димагнийфосфат, а в раствор - свободную фосфорную кислоту. [27]
Исследованием установлено, что образование магнийаммоний-фосфата в процессе нейтрализации протекает в две стадии - сначала до рН 4 8 осаждается димагнийфосфат MgHPO4 ЗН2О, который затем при рН - 6 и выше перекристаллизовывается в магнийаммонийфосфат. [28]
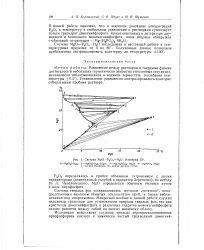 |
Система MgO - Р2О5 - Н2О. Изотерма 25е. [29] |
В нашей работе показано, что в широком диапазоне концентраций Р2О5 и температур в стабильном равновесии с растворами существует только тригидрат димагнийфосфата. [30]
Страницы: 1 2 3 4