Димагнийфосфат
Cтраница 3
Выше этой температуры двухводный мономагнийфосфат прекращает свое стабильное существование в контакте с фосфорнокислым раствором, и ветвь безводного мономагнийфосфата пересекается непосредственно с ветвью димагнийфосфата. [31]
С магнием ортофосфорная кислота образует мономагнийфос-фаты Mg ( H2P04) 2, Mg ( H2P04) 2 2Н20, Mg ( H2P04) 2 4Н20 и димагнийфосфат MgHP04 ЗН20; условия существования безводного димагнийфосфата и тримагнийфосфата не уточнены. [32]
С магнием ортофосфорная кислота образует мономагний-фосфаты Mg ( H PO4) 2, Mg ( H2PO4) 2 - 2H2O, Mg ( H2PO4) 2 - 4H2O и димагнийфосфат MgHPO4 ЗН2О; условия существования безводного диагнийфосфата и тримагнийфосфата не уточнены. [33]
С магнием ортофосфорная кислота образует мономагнийфос-фаты Mg ( H2P04) 2, Mg ( H2P04) 2 2Н20, Mg ( H2P04) 2 4Н20 и димагнийфосфат MgHP04 ЗН20; условия существования безводного димагнийфосфата и тримагнийфосфата не уточнены. [34]
 |
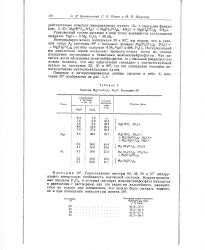
Инвариантные точки системы MgO - РаО6 - Н2О. [35] |
Опытным путем, а также с помощью интер-и экстраполяции исследованы изотермы 0, 10, 50, 58 и 130 тройной системы MgO - РаО5 - НаО, при этом найдено, что в температурном интервале 0 - 130 димагнийфосфат кристаллизуется из фосфорнокислых растворов в виде трехводного кристаллогидрата. [36]
 |
Система MgO - Р2О5 - Н2О. Изотерма 58. [37] |
Что касается ветви насыщения димагнийфосфатом, то с большой уверенностью можно полагать, что она практически совпадает с соответствующей ветвью на изотермах 25, 50 и 80, где это совпадение показано непосредственно экспериментальным путем. [38]
 |
Система MgO - Р2О5 - Н2О. Изотерма 50. [39] |
Результаты даны в табл. 3 и на рис. 4, а. В области с более высоким содержанием Р2О6 в равновесии с растворами находится безводный димагнийфосфат. [40]
Ветвь димагнийфосфата заканчивается в узловой точке А, где раствор содержит 44.8 % Р2О5 и насыщен одновременно двуводным мо-номагнийфосфатом. Интересно, что повышение температуры с 25 до 80 практически не влияет на растворимость трехводного димагнийфосфата. [41]
Полученная этими авторами изотерма состоит из ветвей насыщения трехводным димагнийфосфатом MgHPO4 ЗН2О и мономагнийфосфатом Mg ( H2PO4) 2 - xH2O, гидратность которого авторами не установлена. Камерон и Белл [4] отметили также, что фосфат магния, более основной, чем димагнийфосфат, существует при 25 в равновесии только с крайне разбавленными относительно Р2О5 растворами. Концентрации этих растворов слишком малы, чтобы их можно было определить сколько-нибудь точно. Как мы увидим далее, результаты Камерона и Белла являются достоверными лишь для ветви насыщения димагнийфосфата. [42]
Микроскоп вообще в данной работе служил надежным средством для установления природы твердых фаз, так как кристаллы димагнийфосфата и различных гидратов мономагнийфосфата сильно разнятся между собой по своему внешнему облику. [43]
При содержании 28 7 г Mg ( H2P04) 2 на 100 г Н20 соль без разложения растворяется в воде. Дальнейшее увеличение количества соли на 100 г воды приводит к разложению мономагнийфосфата с выделением в донную фазу трехводного димагнийфосфата. [44]
При соотношении 28.7 г Mg ( H2PO4) 2 на 100 г Н2О соль без разложения растворяется в воде. Дальнейшее увеличение количества соли на 100 г воды приводит к разложению мономагнийфосфата с выделением в донную фазу трехводного димагнийфосфата. Между тем предельное соотношение между монокальцийфосфатом и водой, при котором еще не происходит разложения, составляет 1 г безводной соли на 100 г воды. [45]
Страницы: 1 2 3 4