Реакция - железо
Cтраница 3
По данным измерений оптической плотности строят изомолярные диаграммы оптическая плотность - состав изомолярного раствора при 640 и 700 нм и определяют стехиометрические коэффициенты реакции железа ( II) с 1-нитрозо - 2-нафтолом. [31]
По данным измерений оптической плотности строят изомоляр-ные диаграммы оптическая плотность - состав изомолярного раствора при 640 и 700 нм и определяют стехиометрические коэффициенты реакции железа ( II) с 1-нитрозо - 2-нафтолом. [32]
По данным измерений оптической плотности строят изомолярные диаграммы оптическая плотность - состав изомолярного раствора при 640 и 700 нм и определяют стехиометрические коэффициенты реакции железа ( II) с 1-нитрозо - 2 - нафтолом. [33]
По данным измерений оптической плотности строят изомолярные диаграммы оптическая плотность - состав изомолярного раствора при 640 и 700 нм и определяют стехиометрические коэффициенты реакции железа ( II) с 1-нитрозо - 2-нафтолом. [34]
Большую часть водорода, применяемого в промышленности, в частности при гидрировании растительных масел и китового жира для превращения их в твердые жиры, производят реакцией железа с водяным паром. Водяной пар, поступающий из котла, проходит над нагретой примерно до 600 железной насадкой. [35]
Синий цвет раствора может быть замечен в тех местах, где жидкость дает брызги на стенки, так как реакционная смесь является светонепроницаемой из-за выделяющегося при реакции железа. [36]
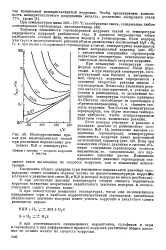 |
Изокоррозионные кривые для низкохромистых сталей при различных парциальных давлениях H2S и температурах. [37] |
При повышении температуры сульфидные пленки становятся более пористыми, и при некоторой температуре, соответствующей пли близкой к экстремальной, скорость коррозии определяется в основном скоростью реакции железа с сероводородом. Чем больше концентрация сероводорода, тем более высокая температура требуется, чтобы контролирующим фактором стала химическая реакция. [38]
Сам Н2О2 не является таким эффективным катодным деполяризатором, как HNO2, поэтому пассивная пленка в присутствии Н2О2 может восстанавливаться только если мгновенная приповерхностная концентрация HNO2, образовавшейся в результате реакции железа и HNO3, достаточно высока. После того как пассивность достигнута, поверхностная концентрация HNOa уменьшается из-за реакции с Н2О2, и ее становится меньше, чем необходимо для поддержания пассивности [ далее цикл повторяется. [39]
Последним областям ( на диаграмме они заштрихованы) соответствуют реакции № 3, 4, 5 и 7 ( на рис. 2.6 они даны в скобках), в ходе которых появляются продукты с низкой растворимостью, Ik электрохимическое равновесие реакций железа влияют величины потенциала и рН, регулируя которые можно вывести систему в область пассивного состояния. [40]
В рассматриваемом способе восстановления ароматических нитросоединений количество используемого же-леза изменяется в зависимости от его вида и степени измельчении так как на скорость восстановления влияет величина активной поиерхности металла [97] Обычно применяют опилки, проходящие череч сито с 80 - 100 отверстиями на 1 сла, из расчета - 200 г на 1 моль иитро-соединеиия Как уже упоминалось, отношение количества соляной кислоты к количеству железа в методе Бешампа всегда ниже стехиометрического, вычисленного из какого-либо приведенного выше уравнения реакции железа с кислотой В промышленных условиях содержание кислоты можно довести до 2 - 3 % от теоретического количества без ущерба для процесса В лабораториях применяют гораздо большие кочнчества кислоты, но не больше 10 % от теоретического. [41]
Данные о реакции железа с перекисью водорода образуют основу взглядов по окислительно-восстановительной активации. [42]
Восстановитель - порошкообразное железо, соединяется с кислородом воздуха, оставшегося в грубке; пары воды, находившиеся в трубке в небольшом количестве, также вступают в реакцию с железом п к трубке создастся слабовосстановительнап атмосфера, которая будет поддерживаться до конца процесса благодаря избытку введенного в реактор железа. За счет образовавшегося при реакции железа с водой водорода произойдет восстановление окислов до СоО, NiO, Mr О, MoOa, WOa. Затем печь выключают и после полного охлаждения трубки полученный окисел пересыпают из лодочки в пробирку и запаивают. [43]
В ряде работ величины энтальпий растворения соединений используют для расчета АЯ / этих соединений в комбинации с АЯ реакций, протекающих в растворах. Для этого были измерены АЯ реакции железа с раствором НС1 и АЯ растворения хлорного железа в соляной кислоте таким образом, что конечные состояния растворов были идентичными. [44]
Перед употреблением катионпт обрабатывают несколько раз 2N НС1 для удаления следов железа. Обработку соляной кислотой заканчивают после исчезновения реакции железа с роданидом аммония. Далее смолу промывают несколько раз дистиллированной водой. [45]
Страницы: 1 2 3 4