Реакция - внутрисферное замещение
Cтраница 2
В начале 1960 - х годов И. И. Черняев [9] подтвердил правильность предположения об образовании промежуточных нитрозо-нитратных соединений. Путем реакций внутрисферного замещения нитратогруппы на координате NO-Pt - N03 был получен ряд интересных по составу и свойствам нитрозосоединений, которые долгое время не удавалось синтезировать. На этих соединениях было доказано, что нитрозогруппа в них обладает значительным трансвлиянием. [16]
Последняя реакция показывает, что трансвлияние МО2 - группы больше, чем хлора или брома, так как в противном случае единственным продуктом реакции должен быть дигалогенокомплекс. Однако генетические соотношения при реакциях внутрисферного замещения, найденные для комплексов двух - и четырехвалентной платины, в химии трехвалентного кобальта оправдываются далеко не всегда. [17]
Характерно, что изменений на NH3 - Pt - NH3 координатах указанных соединений не происходит, что рассматривается как подтверждение низкой величины трансвлияния амми-ногруппы. Этим и объясняется, в частности, высокая устойчивость гексамминов в отношении реакций внутрисферного замещения. Присутствие в молекуле координационного соединения адден-дов, обладающих высокой трансактивностью способствует увеличению ионогенности связи центральный атом - адденд, а, следовательно, и увеличению лабильности внутрисферных групп. В некоторых соединениях, содержащих адденды X, характеризующиеся высокой лабильностью, связь центральный ион - адденд X может носить настолько выраженный ионный характер, что увеличение ионогенности этой связи за счет высокого трансвлияния адденда Y на координате X-центральный ион - Y заметно не сказывается на величине подвижности заместителя X. В этих соединениях могут наблюдаться кажущиеся отклонения от закономерности трансвлияния. [18]
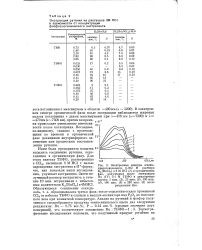
В электронном спектре органической фазы после экстракции наблюдается широкая полоса поглощения с двумя максимумами при Х498 нм ( е - 7300) и Х 470 нм ( е - 7500 нм), причем во време - - j ни происходит уменьшение интенсив - ности полос поглощения. Последнее, по-видимому, связано с протекающими во времени в органической фазе реакциями внутрисферного замещения или процессами восстановления рутения. [20]
Для хрома состояние окисления III является наиболее устойчивым и важным, особенно в водных растворах. Для этого состояния характерно большое число кинетически устойчивых комплексов. Реакции внутрисферного замещения в комплексах Сг111 протекают только в 10 раз быстрее аналогичных реакций комплексов Со111, причем период полураспада обычно бывает порядка нескольких часов. Именно из-за такой кинетической инертности удалось выделить в твердом состоянии большое число комплексных соединений хрома, которые в растворе остаются неизменными в течение длительного времени и часто з условиях, когда они термодинамически нестойки. [21]
Типы комплексных соединений палладия и их свойства во многом похожи на типы и свойства комплексных соединений платины. Однотипные комплексы этих двух элементов ( например, ( NH3) 4PdCl2 - H2O и ( NH3) 4PtCl2 - H2O) изоморфны. Закономерности в изменениях химических ( реакции внутрисферного замещения, превращения, протекающие при нагревании веществ) и физико-химических ( окраска, спектры поглощения, электропроводность растворов и др.) свойств для соединений этих элементов во многом аналогичны. Комплексы Pd ( II) подчиняются закономерности трансвлияния и правилу циклов, а наблюдаемые отклонения от этих правил при переходе от платины к палладию обусловливаются уменьшением ковалентности связи центральный ион - адденд. Разница в свойствах комплексных соединений Pt ( II) и Pd ( II), обусловленная во многом изменением поляризационных свойств при переходе по подгруппам сверху вниз, состоит в следующем. Образование соединений высшей валентности ( 4) для палладия менее характерно, чем для платины. [22]
При этой реакции происходит, очевидно, внедрение атома углерода карбонильной группы ацила в шестичленный цикл с образованием семичленного цикла, в то время как арильныи или алкиль-ный остаток, связанный с карбонильной группсш, становится заместителем при углеродном атоме С7 лиганда. Более подробно механизм этой реакции пока не изучен. Катионы [ С7НбСНзСгС5Н5 ] и С7НбСбН5СгС5Н5 ] также могут быть получены путем реакций внутрисферного замещения из CeHeCrCsHs и метил - или фенил-циклогептатриена в присутствии хлористого алюминия. Взаимодействие СбН6МпС5Н5 с ацилгалогенидами и А1С13 в CS2 также ведет к расширению цикла. [23]
С позицией закономерности трансвлияния комплексные соединения никеля исследованы чрезвычайно мало. Такого рода исследования затруднены, во-первых, вследствие отсутствия данных о строении многочисленных комплексов никеля. Во-вторых, вследствие увеличения ионогенного характера связи металл - адденд при переходе от Pt ( II) к Pd ( II) и Ni ( II), а также в ряду Со ( III) - Ni ( II) внутрисферные заместители в никелевых комплексах довольно лабильны, что сильно усложняет наблюдаемую при реакциях внутрисферного замещения картину. [24]
Страницы: 1 2