Реакция - анион
Cтраница 2
Особое значение имеют реакции анионов с катионами бария и серебра, с которыми они образуют малорастворимые соли. [16]
Таким образом, реакции кротильных анионов в модельных системах приводят к равновесной смеси бутенов, в то время как при полимеризации диенов под влиянием свободных анионов кротильного типа или соответствующих ионных пар реализуется неравновесный процесс, приводящий в основном к структурам, моделирующим а-бутеновое звено Можно сделать вывод, что механизм формирования микроструктур при анионной полимеризации остается пока недо статочно ясным. Следует отметить, что и при свободно-радикальной полимеризации бутадиена образуются полимеры, содержащие равновесные для данной температуры соотношения цис - и транс-звеньев, но количество 1 2-звеньев, составляющее около 20 %, также значительно превосходит рав новесное. [17]
В табл. 12 приведены реакции анионов второй группы. [18]
 |
Реакции анионов третьей аналитической группы. [19] |
В табл. 13 приведены реакции анионов третьей аналитической группы. [20]
 |
Вклады атомов в МО енолят-иона ацетальдегида. [21] |
И действительно, все реакции амбндеитных анионов с электрофильными агентами вдут или по О, или по С ( гл. Важным обстоятельством является тот факт, что в орбиталь ц главный вклад вносит атом углерода С %, а не атом кислорода. Если учесть, что орбитали неподеленных пар электронов атома кислорода лежат инже ф2 ( так как ао ниже ц; см. рис. 2.14), то можно прийти к заключению, что в реакциях с электрофилами, в которых важен орбитальный контроль, будет происходить атака по С, а в реакциях с зарядовым контролем - атака по О ( см. разд. Пустая орбиталь енолят-иона 1з локализуется в основном на С, поэтому по С могла бы ндтн атака нуклеофилами. Однако енолят-анионы не склонны реагировать с нуклеофилами из-за того, что сами имеют отрицательный заряд, т.е. сами являются сильными нуклеофилами. [22]
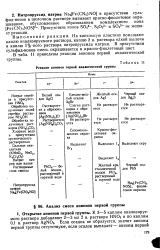 |
Реакции анионов первой аналитической группы. [23] |
В табл. 11 приведены реакции анионов первой аналитической группы. [24]
Описаны два способа проведения реакции аниона SbCl с родамином С. [25]
Как влияет сольватация образующихся в реакции анионов на скорость реакции дегазации. [26]
Макоша и сотрудники подробно изучили реакции анионов бензилцианидов. [27]
Таким образом, константа гидролиза для реакции аниона с водой представляет собой не что иное, как отношение Кн о к константе ионизации слабой кислоты, являющейся продуктом этой реакции. [28]
Эта формула заставляет предполагать участие в реакции единственного аниона и показывает, что только форма ( II) способна образовать такой комплекс. [29]
Отсюда можно полагать, что в реакциях аниона первого типа электрофильный реагент будет вступать в молекулу в экваториальное положение, тогда как в реакциях аниона второго типа - в аксиальное. [30]
Страницы: 1 2 3 4