Реакция - ионизация - водород
Cтраница 1
Реакции ионизации водорода и кислорода тесным образом связаны с процессами их адсорбции на металлах-катализаторах в растворах электролитов. [1]
Количественное изучение реакции ионизации водорода на полудогруженных электродах простейшей формы из металлов платиновой группы, хорошо адсорбирующих водород, было проведено в работах [1, 2] в связи с выяснением механизма токообразующих процессов в пористых электродах топливных элементов. При использовании высокоактивного платинового электрода ( с фактором шероховатости а - 100) в растворах серной кислоты [1] и активного никелевого электрода в растворах щелочи [2] было установлено, что ток ионизации пропорционален периметру трехфазной гра -: ницы металл - газ - электролит. [2]
По отношению к реакции ионизации водорода высокоактивными катализаторами являются сильно адсорбирующие водород металлы - палладий, платина, никель Ренея. Никель Ре-нея относится к так называемым металлам Ренея, которые получают выщелачиванием активного компонента из его сплава с более благородным металлом. Ренея получают выщелачиванием алюминия из Ni - А1 сплава. [3]
По отношению к реакции ионизации водорода высокоактивными катализаторами являются сильно адсорбирующие водород металлы - палладий, платина, никель Ренея. Никель Ре-нея относится к так называемым металлам Ренея, которые получают выщелачиванием активного компонента из его сплава с более благородным металлом. В частности, никель Ренея получают выщелачиванием алюминия из № - А1 сплава. [4]
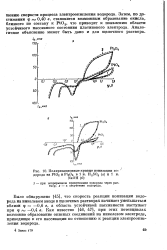 |
Поляризационные кривые ионизации водорода на РЮ2 nPts04 в 1 н. H2SO, ( а и 1 н. NaOH ( б. [5] |
Было обнаружено [45], что скорость реакции ионизации водорода на никелевом аноде в щелочных растворах начинает уменьшаться вблизи ф - 0 6 в, а область устойчивой пассивности наступает при ф я - 0 4 в. Как известно [ 46, 47, при этих потенциалах возможно образование окисных соединений на никелевом электроде, приводящее к его пассивации по отношению к реакции электроокисления водорода. [6]
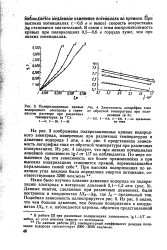 |
Поляризационные кривые [ IMAGE ] Зависимость логарифма тока водородного электрода в серно - от обратной температуры при поля-кислом растворе при различных ризации ( в в. [7] |
По данным работы [21], температурный коэффициент реакции ионизации водорода соответствует 2000 - 3000 кал / моль. [8]
Изучение каталитических свойств дисперсных сплавов палладий-кадмий и палладий-медь в реакциях электрохимической ионизации водорода и кислорода в кислых и щелочных растворах является продолжением исследований физико-химических свойств бинарных систем на основе палладия. Подобная методика снижает до минимума влияние диффузии газа на кинетику изучаемых процессов. Подробно приготовление электродов и проведение измерений описано в работе [1] на примере исследования ионизации и выделения водорода на гидрофобизированной дисперсной платине. [9]
Совокупность всех полученных результатов позволяет объяснить пассивацию платинового электрода по отношению к реакции ионизации водорода следующим образом. [10]
Методом измерения поляризационных кривых гидрофобных электродов определена электрокаталитическая активность дисперсных сплавов палладий-кадмий и палладий-медь в реакциях ионизации водорода и кислорода в кислых и щелочных растворах. Проведено сопоставление свойств сплавов с учетом их относительной поверхности в диапазоне составов: Pd - 33 % ат. [11]
Представлялось интересным получить заведомо нестехиометри-ческие окислы вольфрама, обладающие значительно большей электронной проводимостью, чем WO3, и исследовать их электрокаталитические свойства в реакции ионизации водорода как без платины, так и с платиновым промотором. [12]
Проведен теоретический расчет возможности адсорбции водорода, форм адсорбированного водорода, механизма взаимодействия молекулярного водорода с поверхностью. Рассмотрена термодинамика реакции ионизации водорода и восстановления органических соединений. [13]
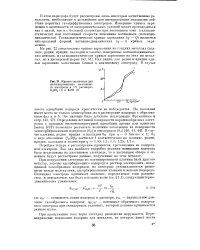 |
Кривые заряжения для платинированного платинового электрода в IN растворах H2S04 ( 1 и КОН ( 2. [14] |
Так как наиболее подробно реакция ионизации водорода была исследована на платиновом электроде, то в настоящем обзоре в основном будут рассмотрены данные, полученные на этом металле. [15]
Страницы: 1 2