Реакция - ионизация - водород
Cтраница 2
Эта реакция является примером окислительно-восстановительных реакций, в которых наряду с переходом электрона происходит перераспределение тяжелых частиц. Действительно, как схематически изображено на рис. 15, реакция ионизации водорода состоит в том, что электрон, который участвовал в образовании химической связи водорода с поверхностью, становится чисто металлическим, а ион водорода - протон - переходит в раствор, где соединяется с молекулой воды. Оценки показывают, что связь Н - Н20 практически заморожена, так что вся динамика связана с растворителем. Вероятность перехода протона определяется формулой типа (1.62), но в нредэкспоненте появляется дополнительный множитель, описывающий перекрытие протонных волновых функций. Таким образом, в этом случае удается оправдать формулу Тафеля и предсказать зависимость коэффициента а от перенапряжения. [16]
Эта реакция является примером окислительно-восстановительных реакций, в которых наряду с переходом электрона происходит перераспределение тяжелых частиц. Действительно, как схематически изображено на рис. 15, реакция ионизации водорода состоит в том, что электрон, который участвовал в образовании химической связи водорода с поверхностью, становится чисто металлическим, а ион водорода - протон - переходит в раствор, где соединяется с молекулой воды. Вероятность перехода протона определяется формулой типа (1.62), но в предэкспоненте появляется дополнительный множитель, описывающий перекрытие протонных волновых функций. Таким образом, в этом случае удается оправдать формулу Тафеля и предсказать зависимость коэффициента а от перенапряжения. [17]
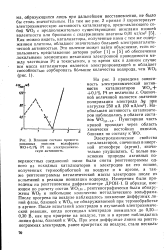 |
Влияние состава промоти-рованных окислов вольфрама WO 0 1 % Pt на электрохимическую активность. [18] |
Электрохимические свойства катализаторов, спеченных в инертной атмосфере ( аргон), значительно ухудшались. С целью выяснения природы активных поверхностных соединений нами были сняты рентгенограммы одного из исходных катализаторов и электродов на его основе, полученных термообработкой на воздухе и в аргоне, а также рентгенограммы каталитической массы электродов после их испытаний в реакции ионизации водорода. Измерения были проведены на рентгеновском дифрактометре ДРОН-1. [19]
Определение порядка реакции ионизации водорода показало, что наблюдается как нулевой [16, 19-22], так и первый [8, 17, 22, 23] порядок. [20]
Поляризация водородного электрода может быть снижена применением катализаторов. Наиболее высокой активностью ( высокий ток обмена) обладают металлы платиновой группы. Электрокаталитическая активность сплавов к реакции ионизации водорода может быть выше каталитической активности отдельных компонентов. [21]
Страницы: 1 2