Реакция - комплексообра-зование
Cтраница 3
Если же ароматический растворитель образует с акцептором прочный комплекс типа ЛУ, подобный комплексу А1Вг3 с мезитиле-ном или комплексу GaCl3 с бензолом, то такое взаимодействие может не только сильно изменять механизм реакции и величины измеряемых параметров, но и препятствовать образованию комплексов акцептора со слабыми донорами. При изучении реакций комплексообра-зования необходимо учитывать возможное взаимодействие компонентов реакции с ароматическим растворителем. Естественно, что сказанное относится не только к системам с галогенами и галогени-дами, но и к системам с другими акцепторами, способными достаточно активно взаимодействовать с ароматическими углеводородами. [31]
Равновесие между ионами металла М, комплексообразующим агентом, или лигандом, X и комплексом зависит от их активностей. В качестве простого примера может служить реакция комплексообра-зования между ионом кадмия и анионом этилендиамин-тетрауксусной кислоты ( ЭДТА) - одним из важнейших реагентов в аналитической химии. [32]
Как видно из уравнения (4.4), в случае образований одноядерных комплексов средняя или суммарная скорость миграции металла не зависит от его общего содержания в растворе при условии, что равновесная концентрация лиганда сохраняется постоянной. Это обстоятельство позволяет использовать электромиграционный метод для исследования реакции комплексообра-зования с участием веществ, находящихся в растворе Б состоянии крайнего разбавления, например искусственных радиоактивных элементов, весовые количества которых труднодоступны или создают сильные радиационные эффекты. [33]
Концентрация свободных ионов радиоактивного изотопа в свою очередь связана с его состоянием в растворе. Так, например, если радиоактивный изотоп участвует в реакциях комплексообра-зования или гидролизуется и образует нерастворимые соединения, то концентрация его свободных ионов уменьшается, потенциал выделения смещается в отрицательную сторону и соответственно уменьшается выделение радиоактивного изотопа на металле. В некоторых случаях оказывается возможным при помощи электрохимического метода отличить истинноколлоидное состояние от псевдоколлоидного. [34]
Емкость поглощения использованных намв: модифицированных сорбентов на основе активного угля ДАУХ еще недостаточно высока. Она зависит от количества комплексообразующего вещества, способного удерживаться носителем, и его доступности для реакции комплексообра-зования и составляет в среднем от 1 до 3 мг-экв / г. Однако при использовании высокоемких носителей ( типа макропористых и изопористых смол) она может быть значительно увеличена. Практически же для тонкой очистки солей марки х.ч. или для извлечения ульграмалых количеств веществ из раствора емкость адсорбционно-комплексообразовательных колонн вполне достаточна; она исчисляется тоннами пропущенного раствора на килограмм сорбента. [35]
Емкость поглощения использованных нами модифицированных сорбентов на основе активного угля ДАУХ еще недостаточно высока. Она зависит от количества комплексообразующего вещества, способного удерживаться носителем, и его доступности для реакции комплексообра-зования и составляет в среднем от 1 до 3 мг-эке / г. Однако при использовании высокоемких носителей ( типа макропористых и изопористых смол) она может быть значительно увеличена. Практически же для тонкой очистки солей марки х.ч. или для извлечения ультрамалых количеств веществ из раствора емкость адсорбционно-комплексообразовательных колонн вполне достаточна; она исчисляется тоннами пропущенного раствора на килограмм сорбента. [36]
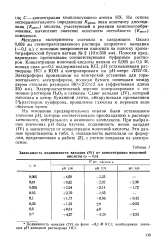 |
Зависимость подвижности ванадия ( IV от концентрации молочной. [37] |
На основе экспериментального определения Кравн, зная константу диссоциации ( ТСдисс) кислоты, участвующей в реакции комплексообра-зования, вычисляют значение константы нестойкости ( / Сяест) комплекса. [38]
Рассматривая инертные комплексы, удобно систематизировать обсуждение механизмов в зависимости от типа изучаемой реакции. Реакция сольволиза и реакция ана-ции, которые мы рассмотрим в первую очередь, есть не что иное, как обратная и прямая реакции комплексообра-зования, которые уже обсуждались для лабильных комплексов. [39]
 |
Радиусы атомов и ионов щелочных элементов. [40] |
При этом физической основой большинства предлагаемых способов является различие в степени гидратации ионов щелочных металлов и лишь в виде исключения появляются работы по разделению некоторых пар щелочных металлов за счет реакций комплексообра-зования. [41]
В современной аналитической химии органические реагенты широко используют как для разделения, так и определения веществ. Методы анализа основаны на различных химических аналитических реакциях; в гравиметрических методах анализа используют реакции осаждения малорастворимых соединений комплексов и солей, для фотометрических методов анализа необходимо присутствие в определяемой молекуле хромофорных групп, комплексонометрические методы титрования полностью основаны на реакциях комплексообра-зования. [42]
Реакции комплексообразования имеют важное значение в аналитической химии. Часто эти реакции сочетаются с кислотно-основными, окислительно-восстановительными и осадительны-ми равновесиями. Вопросы равновесий реакций комплексообра-зования многократно будут обсуждаться в различных главах книги. Данный раздел посвящен хелатометрии - методу титри-метрического анализа, в котором используются реакции комплексообразования. [43]
Так, меняя рН водной фазы, можно изменять степень протонизации солей органических кислот или переводить их в эфиры. При изменении формы неорганических соединений используют реакции комплексообра-зования. [44]
Страницы: 1 2 3