Реакция - паровая конверсия
Cтраница 2
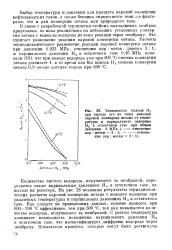 |
Зависимость выхода Н2 при выводе его из зоны реакции паровой конверсии метана от температуры и парциального давления И в остаточном газе при общем. [16] |
В связи с разработкой термически стойких палладиевых мембран предложена, но пока реализована на небольших установках конверсия метана с выводом водорода из зоны реакции через мембрану, dTO сдвигает равновесие реакции паровой конверсии метана. Расчеты термодинамического равновесия реакции паровой конверсии метана при давлении 1 925 МПа, отношении пар: метан равном 6: 1, и парциальном давлении Н2 в остаточном газе O. Mlla показали [18], что при выводе водорода уже при 500 С степень конверсии метана достигает 1, в то время как без вывода Н, степень конверсии метана 0 9 можно достичь только при 880 С. [17]
Однако можно добиться существенной экономии затрат, если часть тепла ископаемых топлив, расходуемого исключительно на поддержание эндотермических реакций, заменить теплом, получаемым от атомных источников. Поскольку и процесс получения водорода, и реакции паровой конверсии, используемые в различных технологических схемах газификации, эндотермичны, можно рассмотреть два основных способа использования атомной энергии при газификации. [18]
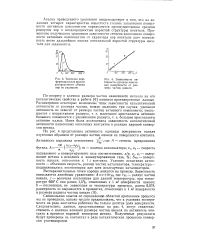 |
Типичная дифференциальная кривая распределения объема пор по радиусам.| Зависимость активности единицы никелевой поверхности от размера частиц никеля. [19] |
По вопросу о влиянии размера частиц нанесенного металла на его каталитические свойства в работе [6] имеются противоречивые данные. Нами была исследована зависимость каталитической активности нанесенных никелевых контактов в реакции паровой конверсии метана. [20]
Таким образом, представляется эффективным технологическое комбинирование производств аммиака, азотной кислоты и спиртов. Кроме того, дальнейшее существенное снижение расхода природного газа может быть достигнуто при использовании в реакции паровой конверсии метана тепла высокотемпературного ядерного реактора. [21]
Бирке и др. [263] предлагают интересную гипотезу дезактивирующего действия воды на алюмоплатиновые катализаторы. По их мнению вода, присутствующая в циркулирующем газе, при температурах риформинга может вступать в реакцию паровой конверсии с углеводородами, давая СО, необходимую для получения карбо-нилхлорида платины. Таким образом, вода может оказывать двоякое отрицательное действие на АПК: удаляет хлор путем гидролиза и способствует уменьшению дисперсности платины. [22]
При введении 0 5м3 водяного пара на 1 м3 кислорода и достижении равновесия отложения углерода не происходит. Однако прак-г тически при газификации образуется углерод в виде сажи. Для упрощения технологического расчета исключают уравнение равновесия реакции паровой конверсии метана, определяющей выход метана, и в расчете учитывают только равновесие реакции конверсии окиси углерода с водяным паром. [23]
Степень стабильности зависит от температуры и парциальных давлений водорода и сероводорода. Это справедливо и для более низких концентраций. Поэтому неудивительно, что оксидные катализаторы чувствительны к отравлению сероводородом, как это наблюдается в синтезе метанола и реакции паровой конверсии оксида углерода. [24]
В табл. 1 приведены характеристики исследованных носителей и катализаторов. Поверхность носителей и катализаторов ( SH, 5K) определяли по методу БЭТ с использованием азота в качестве адсорбата; металлическая поверхность ( SNI) - по хемосорбции окиси углерода при 20 С. Количество никеля в контакте было установлено аналитическим методом. Степень заполнения поверхности активным компонентом ( а) найдена из отношения никелевой поверхности к общей поверхности контакта. Активность всех изученных катализаторов в реакции паровой конверсии метана была оценена проточно-циркуляционным методом. Условия испытания образцов поддерживались постоянными: объемная скорость по метану 1000 ч 1; циркуляция 3 - Ю5 ч - 1; соотношение пар / газ 2: 1, размер частичек 1 - 2 мм, температурный интервал 400 - 800 С. [25]
Страницы: 1 2