Реакция - катионный обмен
Cтраница 2
Катиониты являются высокомолекулярными соединениями - полимерами. Реакции катионного обмена происходят при погружении зерен катионита в раствор электролита. Катиониты могут быть сильнокислотными и слабокислотными. [16]
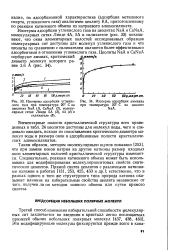 |
Изотермы адсорбции углекислого газа при температуре 20 С на цеолитах NaA ( /, CaNaA ( 2, молекулярных ситах Линде 5А ( 3, 4А ( 4 и силикагеле ( 5. [17] |
Таким образом, методом молекулярных щупов показано [253], что при замене ионов натрия на другие катионы размер входных окон элементарных полостей кристаллической структуры изменяется. Следовательно, реакция катионного обмена может быть использована для модифицирования молекулярноситовых свойств синтетических цеолитов. Прямой синтез цеолитов с различными катионами изложен в работах [ 131, 253, 425, 433 и др. ]; естественно, что в рамках одного и того же структурного типа природа катиона оказывает влияние на избирательные свойства цеолита независимо от того, получен ли он методом ионного обмена или путем прямого синтеза. [18]
При Н - катионировании минерализованность исходной воды оказывает большое влияние на рабочую обменную емкость катионита из-за высокой активности реакций обмена катионов водорода. В результате реакций катионного обмена ионы водорода поглощаются катионитом. При последующей регенерации катионита поваренной солью водород вследствие более высокой активности полностью не вытесняется, и он частично остается в катионите. [19]
Катионит обладает хорошей химической стойкостью и может быть применен для реакций катионного обмена в сильнощелочных средах. [20]
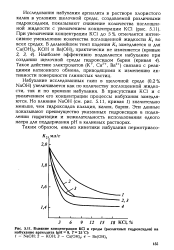 |
Влияние концентрации КС1 и среды ( различных гидроксидов на набухание аргиллита ( рН 9, Т 25 С. [21] |
При увеличении концентрации КС1 до 5 % отмечается интенсивное уменьшение количества поглощенной жидкости К2 во всех средах. Такое действие электролитов ( К, Са2, Ва2) связано с реакциями катионного обмена, приводящими к изменению активности поверхности глинистых частиц. [22]
При этом анионит не способен к реакциям катионного обмена и полностью поглощает анион из фильтруемого раствора кислоты. Когда степень амфотерности равна 100, что возможно при еа0 и ег0, ионит способен только к реакциям катионного обмена. Это означает, что в процессе фильтрования исходного раствора кислоты через регенерированный анионит происходит обогащение фильтрата солями в большем количестве, чем происходит поглощение аниона кислоты. [23]
В таких случаях приведенное выше правило обращается, и Н - катио-ниты проявляют обменную способность, возрастающую прямо пропорционально концентрации названных анионов в Н - катионируемом растворе. При этом выявляются все новые резервы обменных катионов водорода с убывающей потенциальной энергией, которые в обычных условиях не вступают в реакцию катионного обмена. [24]
Рабо и др. [5, 6] провели подобные эксперименты с широкопористыми цеолитами типа У. При нагревании цеолитов ( таким образом было испытано несколько катионных форм цеолитов) в присутствии галогенидов металлов они наблюдали выделение НС1 и связали дегидрогалогенирование с реакцией катионного обмена. Количество выделившегося НС1 зависит от содержания Н в цеолитах. [25]
Поэтому все известные катиониты при эксплуатации их по схеме Na-катио-нирования раствора электролита, как правило, проявляют большую обменную способность, чем при Н - катионировании того же раствора, и менее убывающую с ростом концентрации последнего. Исключением из этого правила являются только те случаи, когда Н - катионируемый раствор электролита содержит анионы, дающие с водородными ионами сочетание, уводящее последние из сферы реакции катионного обмена, как, например, при Н - катионировании щелочных растворов или растворов солей, образованных малодиссоциирующими кислотами. [26]
При полной замене натрия на калий в цеолите NaA на 2 / з снижается адсорбция метанола и резко уменьшается сорбция такого адсорбата, как двуокись углерода. Следует отметить, что калиевый цеолит, синтезированный из гелеобразпого алюмосиликата калия, по своей адсорбционной характеристике ( адсорбция метанола и двуокиси углерода) аналогичен калиевому цеолиту, приготовленному по реакции катионного обмена из натриевого алюмосиликата. [27]
Альдегидные группы определяют используя их восстанавливающую способность. Методы определения карбоксильных групп основаны на реакциях катионного обмена. Кроме химических методов могут также использоваться метод ионообменной хроматографии и спектральные методы. [28]
Свойства ОН-групп, связанных с катионами А13 или Mg2 октаэдрического слоя минералов, в первом приближении приравниваются к свойствам ОН-групп на поверхности гидратиро-ванных А12О3 и MgO. В кислой, нейтральной и даже слабощелочной средах ОН-группы, связанные с катионами А13 и Mg2 на боковых гранях кристаллов минералов, участвуют только в реакциях анионного обмена. Лишь в области значений рН выше изоэлектрической точки ( для а - А12О3 9 2 и MgO 12 5 [86, 88]) протоны ОН-групп, связанные с приповерхностными катионами диоктаэдрических слоев, вступают в реакции катионного обмена. [29]
Страницы: 1 2