Реакция - образование - метанол
Cтраница 1
 |
Метанол из угля. [1] |
Реакция образования метанола из водорода и оксидов углерода является экзотермической, поэтому чрезвычайно важное значение имеет осуществление теплоотвода для устранения перегрева катализатора. Во многих известных процессах синтеза метанола это достигается разными способами - или за счет специальной конструкции реакторов, или особым способом теплоотвода. Ниже рассмотрены наиболее широко используемые процессы производства метанола. [2]
Реакция образования метанола из СО и Н2 является наиболее характерным примером направленного гидрирования монооксида углерода с сохранением связи С-Она типичных оксидных катализаторах. [3]
Механизм реакции образования метанола, несмотря на ее принципиальную простоту, нельзя считать окончательно установленным. [4]
Величина AG реакции образования метанола имеет наибольшее значение и при температуре выше 180 С становится положительной. Так как реакция протекает со значительным уменьшением объема, то высокие давления способствуют смещению равновесия вправо. [5]
Величина AG реакции образования метанола имеет наибольшее начение и при температуре выше 180 С становится положительной, ак как реакция протекает со значительным уменьшением объема, о высокие давления способствуют смещению равновесия вправо. [6]
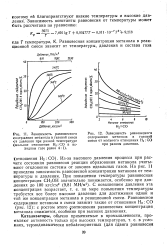 |
Зависимость равновесного содержания метанола в газовой смеси от давления при разной температуре ( мольное отношение Н2. СО в исходном газе равно. [7] |
Из-за высокого давления процесса при расчете состояния равновесия реакции образования метанола учитывают отклонение системы от законов идеальных газов. На рис. 11 приведена зависимость равновесной концентрации метанола от температуры и давления. Равновесное содержание метанола в смеси зависит также от отношения Н2: СО ( рис. 12): с ростом этого соотношения равновесная концентрация метанола снижается, особенно при высоких давлениях. [8]
Из-за высокого давления процесса при расчете состояния равновесия реакции образования метанола учитывают отклонение системы от законов идеальных газов. На рис. 6.2 приведена зависимость равновесной концентрации метанола от температуры и давления. При повышении температуры равновесная концентрация СН3ОН значительно понижается, особенно при давлениях до 20 МПа. Равновесное содержание метанола в смеси зависит также от отношения Н2: СО ( рис. 6.3); с ростом этого отношения равновесная концентрация метанола снижается, особенно при высоких давлениях. [9]
Ле-Шателье, так как из трех указанных выше реакций реакция образования метанола связана с наибольшим уменьшением объема. [10]
На поверхности катализатора формиаты находятся в моноден-татной и бидентатной формах, а реакция образования метанола протекает через лимитирующую стадию гидрирования формиата на меди. [11]
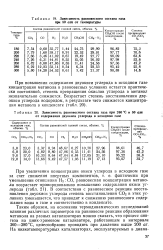 |
Зависимость равновесного состава газа при 50 am от температуры.| Зависимость равновесного состава газа при 260 С и 50 am от содержания двуокиси углерода в исходном газе. [12] |
Таким образом, на основании термодинамических исследований влияния различных параметров на равновесие реакции образования метанола на разных катализаторах можно сказать, что процесс синтеза на цинк-хромовом катализаторе, работающем в интервале 360 - 380 С, целесообразно проводить при давлении выше 200 ат. [13]
Приняв такую точку зрения, естественно, возникает вопрос, почему уравнения скорости реакции образования метанола на цинк-хромовом катализаторе, предложенные различными авторами, применимы только для узкой области концентраций компонентов и, как правило, не описывают результатов экспериментов других исследователей. Скорее всего это объясняется тем, что одновременно с реакцией образования метанола возможен ряд параллельных последовательных реакций, в которых принимают участие как метанол, так и исходные компоненты. Эти побочные реакции протекают на самой поверхности катализатора, хотя не исключается и взаимодействие в близлежащем окружающем его объеме. Кинетические закономерности этих реакций пока не изучены, так как только с развитием хроматографического анализа появилась возможность расшифровать примеси, содержащиеся в метаноле-сырце. [14]
Конверсия синтез-газа за один проход через реактор составляет 15 - 50 % и обусловливается равновесием реакции образования метанола в выбранных условиях, продолжительностью контакта и допустимым перепадом температуры по слою катализатора, при адиабатическом режиме процесса. [15]
Страницы: 1 2 3