Реакция - образование - метанол
Cтраница 2
Это необходимо для поддержания температуры катализатора - 360 - 370 С, так как за счет тепла реакции образования метанола температура газа после прохождения каждой полки или слоя катализатора в шахтной насадке повышается. Температурный режим по высоте колонны приведен на стр. Подача газа по холодным байпасам зависит от активности катализатора и технологических параметров, определяющих скорость образования метанола, а также от условий теплообмена; он колеблется в пределах 10 - 20 % от общего расхода газа. [16]
К катализаторным коробкам колонн для синтеза метанола предъявляются более высокие требования, чем для синтеза аммиака, так как реакция образования метанола должна протекать в более узком температурном интервале. Перегрев же катализатора синтеза аммиака обычно приводит только к снижению его активности и сокращению пробега колонны. [17]
Высказанные выше предположения и выводы сделаны на основании анализа экспериментальных данных, но не подтверждены прямыми исследованиями механизма процесса. Судя по данным большого числа исследователей, реакция образования метанола является сложной, и поэтому вопрос о ее механизме, видимо, будет предметом специального изучения. [18]
Для процесса синтеза метанола предложено много катализаторов, Лучшими из них оказались катализаторы, основными компонентами которых являются окись цинка или медь. Медные катализаторы обладают высокой активностью-уже при температуре около 300 реакция образования метанола протекает с большой скоростью. Чистая окись цинка является относительно малоактивным катализатором. Для производственных условий наиболее пригодны смешанные катализаторы, например цинк-хромовые, которые, как правило, чаще, чем однокомпонентные, обнаруживают избирательные свойства. Железо и никель ускоряют реакции, ведущие к образованию метана. Щелочные окислы ( Na2O, K2O, СаО) даже при незначительной добавке к катализатору вызывают образование высших спиртов. [19]
Приняв такую точку зрения, естественно, возникает вопрос, почему уравнения скорости реакции образования метанола на цинк-хромовом катализаторе, предложенные различными авторами, применимы только для узкой области концентраций компонентов и, как правило, не описывают результатов экспериментов других исследователей. Скорее всего это объясняется тем, что одновременно с реакцией образования метанола возможен ряд параллельных последовательных реакций, в которых принимают участие как метанол, так и исходные компоненты. Эти побочные реакции протекают на самой поверхности катализатора, хотя не исключается и взаимодействие в близлежащем окружающем его объеме. Кинетические закономерности этих реакций пока не изучены, так как только с развитием хроматографического анализа появилась возможность расшифровать примеси, содержащиеся в метаноле-сырце. [20]
Сырьевой газ поступает в верх реактора, нисходящим потоком проходит снаружи слоя катализатора и омывает трубы теплообменника. Затем он поднимается в верх реактора и вновь спускается по слою катализатора, где протекает реакция образования метанола. Поток горячих продуктов реакций проходит по трубам теплообменника, нагревая поступающий сырьевой газ до температуры реакции, и выводится из реактора. [21]
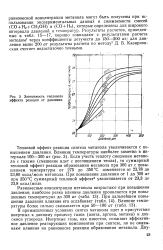 |
Зависимость теплового эффекта реакции от давления. [22] |
Тепловой эффект реакции синтеза метанола увеличивается с повышением давления. Если учесть теплоту смешения метанола с газами ( смешение идет с поглощением тепла), то суммарный тепловой эффект реакции образования метанола при 300 ат с повышением температуры от 275 до 350 С изменяется от 23 78 до 23 80 ккал / моль метанола. При повышении давления от 1 до 300 ат при 350 С суммарный тепловой эффект8 увеличивается от 23 3 до 23 8 ккал / моль. [23]
 |
Зависимость теплового эффекта реакции от давления. [24] |
В промышленных условиях синтез метанола идет в присутствии инертных к данному процессу газов ( азота, аргона, метана) и двуокиси углерода. Инертные газы, как известно, снижают эффективное давление реагирующих компонентов при синтезе, но не оказывают влияния на равновесие реакции образования метанола. [25]
 |
Зависимость равновесного состава газа при 380 С и 300 am. [26] |
Интересно рассмотреть изменение равновесных концентраций компонентов в условиях производства метанола при 50 ат на низкотемпературных медь-цинк-алюминиевых катализаторах. Для расчета принят следующий состав газовой смеси на входе в колонну синтеза: 16 объемн. При расчете учитывалось, что одновременно с реакцией образования метанола идет реакция восстановления СО2 водородом. [27]
Для процесса синтеза метанола предложено много катализаторов. Лучшими из них оказались катализаторы, основными компонентами кото рых являются окись цинка или медь. Медные катализаторы обладают высокой активностью-уже при температуре около 300 реакция образования метанола протекает с большой скоростью. Чистая окись цинка является относительно малоактивным катализатором. Для производственных условий наиболее пригодны смешанные катализаторы, например цинк-хромовые, которые, как правило, чаще, чем однокомпонентные обнаруживают избирательные свойства. Железо и никель ускоряют реакции, ведущие к образованию метана. Щелочные окислы ( Na2O, K2O, СаО) даже при незначительной добавке к катализатору вызывают образование высших спиртов. [28]
В верхней части колонны установлена катализаторная коробка, заполняемая испытуемым катализатором. Нагретая з-а счет тепла отходящих прореагировавших газов и самой реакции смесь попадала в верхнюю часть колонны в зону катализатора, где и осуществлялась реакция образования метанола. [29]
 |
Зависимость равновесной степени превращения СО от давления. [30] |
Страницы: 1 2 3