Реакция - образование - силикат
Cтраница 2
 |
Изменения теплоемкости при температуре полиморфных превращений. [16] |
Тепловой эффект, сопровождающий реакцию образования силиката из отдельных составляющих его окислов, измеряют различными способами. Чаще всего сравнивают теплоты растворения окислов, взятых в свободном состоянии, с теплотой растворения готового силиката. При этом следует вносить поправки на изменение теплот реакций в зависимости от температуры. [17]
Подобным же образом советский ученый А. С. Бережной детально изучил реакции образования силикатов в твердой фазе в системе MgO - СаО - SiOa. [18]
Протекает также и непосредственное взаимодействие исходных карбонатов с оксидом кремния. При 750 - 900 С ( в результате плавления эвтектических смесей двойных солей с карбонатом натрия) возникает жидкая фаза, и поэтому реакция образования силикатов ускоряется. При дальнейшем нагревании разлагается еще не вступивший в реакцию карбонат кальция, образовавшийся оксид кальция и оставшаяся сода взаимодействуют с оксидом кремния на поверхности его частиц, а остаток оксида SiO2 постепенно растворяется в расплаве силикатов. Небольшая добавка к шихте плавикового шпата CaF2 ускоряет процесс варки стекла. [19]
Опыты 1956 г. показали, что принятая 30 лет назад Таманном гипотеза образования силиката кальция может быть очень просто проверена и доказана. Оказалось, что при измельчении кристаллов кальция с силикагелем в вакуумной шаровой мельнице при комнатной температуре с выделением двуокиси углерода имеет место очень ясно выраженная реакция образования силиката кальция. Даже при измельчении горного хрусталя с исландским полевым шпатом в вакууме можно наблюдать значительно повышенное по сравнению с наблюдаемым при размоле одного лишь кальцита выделение двуокиси углерода. [20]
На примере реакций диссоциации карбонатов и дегидратации некоторых гидроксидов, твердофазового синтеза силикатов, алюминатов и других тугоплавких веществ была выявлена возможность ускорения соответствующих реакций в пределах от 5 до 300 раз. Об этом свидетельствуют данные, суммированные в табл. 23, а также приведенные в табл. 24, показывающие зависимость степени превращения от продолжительности термообработки в реакциях образования силикатов кальция, являющихся основными минералами портландцементного клинкера. [21]
Протекает также и непосредственное взаимодействие исходных карбонатов с двуокисью кремния. При 750 - - 900 С ( в результате плавления эвтектических смесей двойных солей с карбонатом натрия, а затем и самого карбоната натрия) возникает жидкая фаза, и поэтому реакция образования силикатов ускоряется. При дальнейшем нагревании разлагается еще не вступивший в реакцию карбонат кальция, а образовавшаяся окись кальция и оставшаяся сода взаимодействуют с двуокисью кремния на поверхности ее частиц, а остаток двуокиси кремния постепенно растворяется в расплаве силикатов. Небольшая добавка к шихте плавикового шпата CaF2 ускоряет процесс варки стекла. [22]
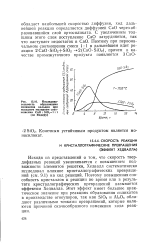 |
Последовательность образования силикатов кальция при исходном молярном соотношении СаО. SiO2l. 1 ( по Яндеру. [23] |
Исходя из представлений о том, что скорость твердофазных реакций увеличивается с повышением подвижности элементов решетки, Хедвалл систематически исследовал влияние кристаллографических превращений ( см. 9.1) на ход реакций. Поэтому повышенная способность кристаллов к реакции во время или в результате кристаллографических превращений называется эффектом Хедвалла. Этот эффект имеет большое практическое значение при реакциях образования силикатов в производстве огнеупоров, так как SiO2 и А12О3 обладают различными точками превращений, которые являются причиной скачкообразного изменения хода реакции. [24]
Варка стекломассы - это совокупность сложных физико-химических процессов, протекающих в гетерогенной системе через стадии собственно варки, осветления ( гомогенизации) массы и ее охлаждения. Эти процессы начинаются в твердой фазе до расплавления шихты и продолжаются в расплаве. Скорость процесса варки в значительной степени зависит от скорости диффузии компонентов как в твердой, так и в жидкой фазах. В твердой фазе протекают реакции образования силикатов, в жидкой при температуре 1200 - 1240 С - процессы стеклообразования. В табл. 20.3 представлена последовательность процессов, протекающих при варке стекломассы с изменением температуры. [25]
По мнению авторов, отмеченный выше замедляющий эффект является результатом физико-химического взаимодействия частиц шлака и песка в момент их дробления. Петере указывает, что в процессе измельчения твердых материалов происходят процессы не только в смысле физики измельчения, но что эти процессы в очень многих случаях сопровождаются химическими превращениями. При воздействии сил на твердые вещества могут наблюдаться все виды реакций, известные из химии твердых тел. Петере, ссылаясь на опыты 1956 г., отмечает, что в процессе измельчения кристаллов карбоната кальция с силикагелем в вакуумной шаровой мельнице при комнатной температуре имеет место ярко выраженная реакция образования силиката кальция. [26]
Следовательно, число независимых реакций равно разности между общим числом компонентов с учетом условно введенных свободных элементов, если они не присутствуют в системе, и числом элементов, из которых эти вещества могут быть образованы. Последнее соотношение позволяет избежать ошибок тогда, когда структурные элементы определены неправильно. Если же за элементы принять атомы, то У 3, a k 9, поскольку появятся гипотетические Са, О, Si. В данном случае W 9 - 3 6 и к 4 - м реакциям образования силикатов следует прибавить две реакции диссоциации окислов. [27]
Страницы: 1 2