Реакция - окисление - ацетальдегид
Cтраница 1
Реакция окисления ацетальдегида в уксусную кислоту протекает несколько сложнее, чем это указано на стр. [1]
Реакция окисления ацетальдегида в уксусную кислоту протекает несколькэ сложнее, чем это указано на стр. [2]
Реакция окисления ацетальдегида в уксусную кислоту протекает несколько сложнее, чем это указано на стр. [3]
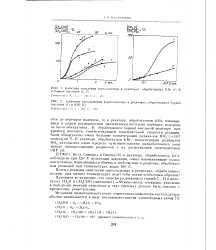 |
Кинетика окисления ацетальдегида в реакторах, обработанных КВг ( /, 4 и борной кислотой ( -, 3.| Кинетика расходования формальдегида в реакторах, обработанных борной кислотой ( Л и КВг ( 2. [4] |
Почему реакция окисления ацетальдегида в реакторах, обраоотанных солями, при низких температурах ведет себя таким необычным образом. [5]
Получают на основе реакции окисления ацетальдегида. [6]
 |
Новые хемилюминесцентные реакции в газовой фазе. [7] |
Наиболее подробно исследована хемилюминесценция в реакции окисления ацетальдегида. При окислении ацетальдегида образуются продукты простого строения, что облегчает идентификацию возбужденных частиц. [8]
Какую роль играет катализатор в реакции окисления ацетальдегида в уксусную кислоту. [9]
Показано, что тяжелые побочные продукты реакции окисления ацетальдегида влияют на первую стадию процесса. Добавленные в небольшом количестве, они вызывают увеличение скорости реакции, при дальнейшем увеличении их содержания в растворе скорость реакции падает. [10]
Основными компонентами раствора при промышленном осуществлении реакции окисления ацетальдегида являются: уксусный ангидрид, уксусная кислота, ацетальдегид, вода, переки. Катализатором этого процесса служит смесь ацетатов меди и кобальта. [11]
Образование возбужденного формальдегида свидетельствует о том, что реакция окисления ацетальдегида идет с участием мето-ксильных и гидроксильных радикалов. Указания на участие этих радикалов в процессе окисления могут быть получены из данных химического анализа. В ходе реакции ( после полного потребления кислорода) наблюдается появление метана и этана, что возможно только при наличии в системе метильных радикалов. [12]
В дальнейшем кинетический метод был успешно использован для изучения промежуточных соединений в реакциях окисления ацетальдегида [39], пропилена [41, 40], изобутана [41], пропана [42] и, в частности, для выяснения механизма гомогенного катализа окисления пропана бромистым водородом [43] ( см. стр. [13]
Выяснение механизма образования возбужденных молекул формальдегида позволяет подойти к объяснению сложного характера кинетических кривых хемилюминесценции в реакции окисления ацетальдегида. [14]
В результате ф, / - g, где / и g - кинетические коэффициенты реакций разветвления цепи и гетерогенной и гомогенной гибели радикалов для реакторов, обработанных KCI и КВг, оказывается больше, чем ф2 для реакции окисления ацетальдегида в реакторах, обработанных борной кислотой или реакцией. Следует ожидать наличие такой температуры, при которой ф ] ж фа и, следовательно, максимальные скорости, измеренные во всех реакторах, будут одинаковыми. Такой температурой, как было показано, является 225 С. [15]
Страницы: 1 2