Реакция - глубокое окисление
Cтраница 3
Видно, что выше 270 - 300 начинают идти реакции глубокого окисления и окислительного дегидрирования. Дальнейшее повышение температуры приводит к резкому падению селективности. [31]
Наряду с окислительным дегидрированием олефина на этом катализаторе протекают реакции глубокого окисления до СО2 и изомеризации до - цис - и - транс-бутиленов. [32]
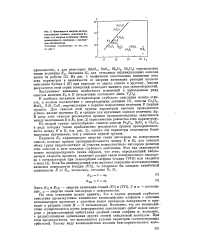 |
Зависимость энергии активации реакции полного окисления бу-тена-1 от энергии активации обмена молекулярного кислорода с кислородом катализатора. [33] |
На этом основании можно принять, что в случае реакций глубокого окисления промежуточное химическое взаимодействие олефинов с окисным катализатором протекает с участием ионов кислорода поверхности и приводит к разрыву связи М - О катализатора. Возможно, что это взаимодействие осуществляется путем перекрывания заполненных орбит ионов кислорода с разрыхляющими орбиталями двойной связи олефина и, возможно, с разрыхляющими орбиталями других связей окисляемой молекулы. При этом предполагается, что выполняется условие симметрии соответствующих орбиталей. [34]
Наиболее вероятной причиной низкой каталитической активности этих окислов в реакциях глубокого окисления является большая энергия связи поверхностного кислорода, что вытекает из высоких значений для них параметра EQ. В то же время для окислов третьей группы характерна наибольшая избирательность каталитического действия в отношении реакций окисления олефинов по С - Н - связи. Следовательно, лимитирующим этапом в этих условиях становится стадия ( VII), включающая взаимодействие катализатора с оле-фином. Однако установленная для окислов третьей группы независимость Е от ЕО свидетельствует об ином для них механизме промежуточного химического взаимодействия с олефином. В рассматриваемом случае это взаимодействие уже не связано с отрывом кислорода от поверхности окисла. В этом, вероятно, состоит основное отличие механизма катализа окисления олефинов по С - Н - связи от механизма их глубокого окисления. [35]
Растворенный в палладии кислород существенно снижает его активность в реакциях глубокого окисления. По-видимому, уменьшение каталитической активности металлов под действием кислорода является общей закономерностью. [36]
На катализаторах, содержащих двухвалентную медь, главным образом протекают реакции глубокого окисления. [37]
В работе [114] установлена корреляция между реакционной способностью углеводородов в реакции глубокого окисления на оксидных катализаторах и стандартной энергией Гиббса окислительной реакции, отнесенной к единице условного продукта. [38]
На рис. 27 представлена зависимость удельной каталитической активности веществ в реакции глубокого окисления пропилена при 300 С от величины энергии связи кислород - катализатор. Наблюдаемое уменьшение скорости реакции с увеличением qs согласуется с представлением о том, что процесс протекает по схеме попеременного восстановления - окисления поверхности, причем в медленной стадии происходит разрыв связи кислород - катализатор. [39]
При повышении температуры ускоряются побочные реакции, тепловой же эффект реакции глубокого окисления более чем в тринадцать раз превышает тепловой эффект полезной реакции. Необходимо эффективное регулирование температуры, предотвращающее ее быстрое повышение и снижение выхода окиси этилена. [40]
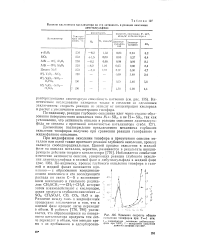 |
Удельная скорость общего окисления тиоэфиров при Г1 атм. [41] |
При жидкофазном окислении тиоэфира в присутствии окислов металлов или солей также протекает реакция глубокого окисления, процесс является свободнорадикалъным. По-видимому, процесс глубокого окисления тиоэфира в газовой и жидкой фазах начинается одинаково - с образования координационного комплекса И его последующего распада по связи С-S с возникновением алкильного и тиильного радикалов: CH3SCH3 - vCH3 CH3S, которые затем взаимодействуют с кислородом, давая продукты глубокого окисления - j SO СНзЗОзН, СО, СО2, Н2О и др. Различие между газо - и жидкофазным процессами заключается в том, что в жидкой фазе процесс легче переходит в объем. [42]
 |
Корреляция реакционной способности R и изменения энергии Гиббеа в реакции глубокого окисления углеводородов при 300 С и концентрации углеводородов 2 % ( об.. [43] |
На рис. 18 представлена зависимость реакционной способности различных углеводородов от энергии Гиббеа реакции глубокого окисления для ряда оксидных катализаторов. [44]
 |
Корреляция реакционной способности R и изменения энергии Гиббса в реакции глубокого окисления углеводородов при 300 С и концентрации углеводородов 2 % ( об.. [45] |
Страницы: 1 2 3 4