Реакция - оксиэтилирование
Cтраница 3
Патат, Кремер и Боблетер26 28 исследовали кинетику обеих стадий реакции оксиэтилирования фенола, а именно образование фенилмоно - и фенилдиэтиленгликолевого эфиров. Энергия активации первой стадии составляет 15 8 0 2 ккал / моль, второй стадии - 16 4 0 2 ккал / моль. Эти исследователи также установили, что до тех пор, пока в зоне реакции имеется свободный фенол, образуется исключительно моногликолевый эфир. Однако полученные ими результаты не всегда соответствуют бимолекулярной реакции, а обработанные ими данные привели к выводам. При обработке этих экспериментальных данных Лове и Вейбе - лом29 получилось, что реакция между феноокси-ионом и окисью этилена соответствует реакции первого порядка. По мере использования фенола скорость реакции снижается, однако она снова увеличивается, когда начинается взаимодействие фенилгликоле-вого эфира с окисью этилена. Возможно, что имеет место тримолекулярная реакция. Такое предположение было сделано Лоури30 для объяснения превращений тетраметил глюкозы. [31]
Приведены значения констант скорости, температурного коэффициента скорости и энергии активизации реакции оксиэтилирования указанных соединении. [32]
Из полученных данных по энергии активизации можно заключить, что в исследуемых условиях реакция оксиэтилирования проходит в диффузионной области. [33]
Перечисленные свойства этого катализатора обуславливают все более широкое использование его для промышленного осуществления реакции оксиэтилирования различных. Вместе с тем в литературе отсутствуют данные по относительной каталитической активности эфирата фтористого бора в реакциях с различными спиртами в сопоставимых условиях, что затрудняет оценку перспективы его использования в различных синтезах. [34]
Перечисленные свойства этого катализатора обуславливают все более широкое использование его для промышленного осуществления реакции оксиэтилирования различных спиртов. Вместе с тем в литературе отсутствуют данные по относительной каталитической активности эфирата фтористого бора в реакциях с различными спиртами в сопоставимых условиях, что затрудняет оценку перспективы его использования в различных синтезах. [35]
К второй группе вопросов относятся теоретические вопросы, связанные с распределением полимергомологов по молекулярному весу ( полидисперсностью) при реакции оксиэтилирования. Число экспериментальных работ в этой области очень ограничено. [36]
В технических образцах оксиэтилированных НПАВ, независимо от способа их получения, присутствуют в качестве примесей полиэтиленгликоли ( ПЭГ) - побочный продукт реакции оксиэтилирования, а также непрореагировавшие исходные вещества и продукты разложения катализаторов. [37]
Сп - концентрация реагирующего вещества в слое, прилегающем к границе раздела фаз; D - коэффициент диффузии, зависящий от температуры. Если реакция оксиэтилирования находится в диффузионной области, то в результате поддержания постоянного давления окиси этилена в реакторе скорость диффузии, а следовательно, и скорость всей реакции будет оставаться при данной температуре постоянной. [38]
Поликонденсация основана на принципе одинаковой реакционной способности функциональных групп как в мономере, так и в полимере. В реакции оксиэтилирования полимергомологи образуются в результате присоединения окиси этилена к реакцион-носпособным соединениям. Реакционноспособность одних и тех же функциональных групп на всех стадиях процесса остается одинаковой ( стр. [39]
Отсюда следует, что если реакционная способность концевых гидроксильных групп одинакова, то скорость оксиэтиро-вания не будет зависеть от концентрации оксиэтилируемого соединения и будет определяться только концентрацией окиси этилена. Как известно [1-7], реакция оксиэтилирования является реакцией первого порядка. [40]
Краткие сведения о механизме реакции приведены ранее, при описании отдельных классов соединений. В присутствии щелочных катализаторов реакции оксиэтилирования различных классов соединений протекают следующим образом. [41]
Определенный интерес представляет подход к этому явлению с позиций уравнения Бренстеда, где каталитическое действие кислот ставится в зависимость от их силы. С этой целью были проведены исследования реакции оксиэтилирования аминов при катализе различными по активности карбоновыми кислотами. [42]
Иминный водородный атом амидной связи подвижен и может быть замещен на различные радикалы. На этом основаны многочисленные реакции полиамидов, например реакция оксиэтилирования, которая приводит к получению производных с ценными свойствами. [43]
Основываясь на ранее проведенных авторами работах [10, 11] по оксиэтили-рованию соединений, полученных на основе чистых реактивов, и работах, выполненных другими исследователями [12] по оксиэтилированию соединений с несколькими гидрофобными и гидрофильными цепями, кинетика оксиэтилирования изучалась в температурном интервале 140 - 200 Сив присутствии 2 % вес. Выбор последнего связан с тем, что он является одним из наиболее активных и недифицитных катализаторов реакции оксиэтилирования. [44]
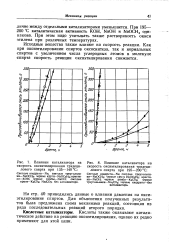 |
Влияние катализатора на скорость оксиэтилирования тридеци.| Влияние катализатора на скорость оксиэтилирования тридеци. [45] |
Страницы: 1 2 3 4