Реакция - будуар
Cтраница 1
Реакция Будуара эндотермическая, и равновесие должно сместиться влево, т.е. должно образовываться больше СО2 и С, если нет препятствий зародышеобразованию. [1]
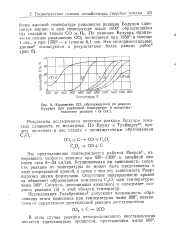 |
Количество СО, образующегося по реакции. [2] |
По реакции Будуара практически полное разложение СО2 достигается при 1250 в течение 1 сек. [3]
Скорость реакции Будуара для древесного угля, измеренная в циркуляционной установке при различных условиях. [4]
 |
Схематическое представление возможных путей образования углерода согласно теориям полимеризации углеводородов. [5] |
Теория реакции Будуара предложена в [131, 132], Предполагается, что в пламени предварительно перемешанных смесей углерод образуется по реакции 2СО СО2 С. [6]
Состояние равновесия реакции Будуара в условиях хлорирования брикетов из оксида ванадия и угля, как правило, не достигается. [7]
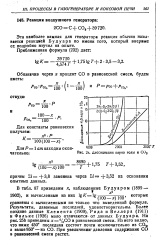
Восстановление диоксида углерода углеродом (5.141) часто называют реакцией Будуара, а характерные S-образные кривые на рис. 5.7 - кривыми Будуара. [8]
 |
Диссоциация паров воды и CUS. [9] |
Эта наиболее важная для генератора реакция обычно называется реакцией Будуара по имени того, который впервые ее. [10]
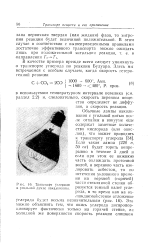 |
Транспорт углерода в угольной лампе накаливания. [11] |
В качестве примера прежде всего следует упомянуть о транспорте углерода по реакции Будуара. [12]
Выбор р независимых реакций произволен, но, как было показано при изучении реакции Будуара, рациональность при этом может значительно упростить расчеты, так как для выбранного базиса реакций значение по крайней мере одной координаты реакции становится очевидным. Теперь обратимся к следующей задаче: даны два возможные базиса независимых реакций; если найдены координаты реакции, соответствующие одному базису, то каковы значения координат реакции другого базиса. [13]
Нежелательными ( побочными) реакциями следует считать гидрирование СО в метан, разложение СО на углерод и С02 ( реакция Будуара) и окисление металла водой и диоксидом углерода. [14]
Это положение справедливо и для скорости установления равновесного состояния в гетерогенной системе: небольшая по величине скорость установления равновесного состояния в реакции Будуара может быть объяснена большим значением энергии диссоциации молекул СО. [15]
Страницы: 1 2 3