Реакция - нулевой порядок
Cтраница 2
Для реакции нулевого порядка скорость превращения не зависит т концентрации реагента. Следовательно, если при гр концентрация имеет конечное значение, фактор эффективности равен единице. [16]
Для реакции нулевого порядка х - хь независимо от величины т и, следовательно, степень превращения зависит только от общего времени пребывания. [17]
Для реакции нулевого порядка получим результат, аналогичный модели ( Ь - т), так как х хь не зависит от степени перемешивания. [18]
Существуют реакции нулевого порядка, например разложение некоторых соединений на поверхности различных веществ, когда скорость распада веществ не зависит - от их концентрации в объеме, и реакции дробного порядка, например при многостадийных процессах, если самые медленные стадии имеют разный порядок, но скорости их соизмеримы. Разумеется, ни нулевой, ни дробной мо-лекулярности быть не может, так как она относится к механизму реакции, а не к описывающему ее уравнению. [19]
Существуют реакции нулевого порядка, например разложение некоторых соединений на поверхности различных веществ, когда скорость распада веществ не зависит от их концентрации в объеме, и реакции дробного порядка, например при многостадийных процессах, если самые медленные стадии имеют разный порядок, но скорости их соизмеримы. Разумеется, ни нулевой, ни дробной мо-лекулярности быть не может, так как она относится к механизму реакции, а не к описывающему ее уравнению. [20]
Для реакции нулевого порядка, проводимой при постоянной температуре, t скорость не зависит от концентрации. [21]
Для реакции нулевого порядка х - хь независимо от величины т и, следовательно, степень превращения зависит только от общего времени пребывания. [22]
Для реакции нулевого порядка получим результат, аналогичный модели ( Ь - т), так как х хь не зависит от степени перемешивания. [23]
Для реакции нулевого порядка производительность катализатора есть пели чина поггошшан, а степень превращения обратно пропорциональна объемной скорости. [24]
Существуют реакции нулевого порядка, например разложение некоторых соединений на поверхности различных веществ, когда скорость разложения не зависит от концентрации соединения в объеме. Некоторые многостадийные процессы, в которых самые медленные стадии имеют разный порядок, но скорости их соизмеримы, представляют собой реакции дробного порядка. Разумеется, ни нулевой, ни дробной молекулярности быть не может, так как она относится к механизму реакции, а не к описывающему ее кинетическому уравнению. [25]
Для реакции нулевого порядка получим результат, аналогичный модели ( Ь - т), так как ххь не зависит от степени перемешивания. [26]
Для реакции нулевого порядка х хь независимо от величины т и, следовательно, степень превращения зависит только от общего времени пребывания. [27]
Для реакции нулевого порядка получим результат, аналогичный модели ( Ь - т), так как х хь не зависит от степени перемешивания. [28]
Для реакции нулевого порядка х - хь независимо от величины т и, следовательно, степень превращения зависит только от общего времени пребывания. [29]
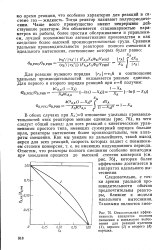 |
Относительная эффективность аппаратов полного смешения и идеального вытеснения для реакций нулевого ( /, первого ( 2 и второго ( 3 порядка. [30] |
Страницы: 1 2 3 4