Реакция - разложение - пероксид - водород
Cтраница 1
Реакция разложения пероксида водорода в кислом растворе 2Н О2 2Н2О О2 ускоряется бромид-ионами. [1]
Реакция разложения пероксида водорода в кислом растворе 2Н О2 - 2Н - О О2 ускоряется бромид-ионами. [2]
 |
Аналитические характеристики индикаторных реакций для определения железа ( окислитель - персульфат и периодат. [3] |
Реакция разложения пероксида водорода, катализируемая ионами железа, протекает в щелочной среде. [4]
Для реакции разложения пероксида водорода, катализируемого ионами СгаОГ, было обнаружено, что при изменении температуры процесса от 0 до 56 С определенный экспериментально порядок реакции изменяется от нулевого до второго. [5]
Тепловой эффект реакции разложения пероксида водорода равен - - 97 01 кДж / моль. [6]
Написать уравнение реакции разложения пероксида водорода К какому типу окислительно-восстановительных реакций она относится. [7]
Предположение оказалось верным, реакция разложения пероксида водорода является реакцией лервого порядка. [8]
Из этого выражения следует, что скорость реакции разложения пероксида водорода и соответственно образования кислорода должна быть прямо пропорциональна начальной концентрации катализатора. Постарайтесь ответить, как должна зависеть скорость реакции от концентрации пероксида водорода. [9]
Задачи работы: аналитически определить константу скорости реакции разложения пероксида водорода на платине; построить графическую зависимость в координатах: объем выделенного кислорода ( VQ) - время t и определить период полупревращения. [10]
Для изучения каталитических свойств платины на цеолитах была выбрана реакция жидкофазного разложения пероксида водорода. [11]
Таким образом, число возможных элементарных реакций, из которых складывается реакция разложения пероксида водорода, очень велико: отсутствие же надежных экспериментальных методов обнаружения промежуточных активных частиц приводит к тому, что механизмы реакции являются гипотетическими. [12]
Исследование влияния различных факторов на каталитическую активность ионитных комплексов, а также нанесенных на иониты комплексов в реакциях жидкофазного разложения пероксида водорода, пиридилэтилирования аминов, конденсации, гидрирования, изомеризации двойной связи, окисления - восстановления и других позволило установить принципиальную возможность целенаправленного синтеза каталитически-активных систем регулированием состава среднестатистического кооринационного центра, изменением микро - и макроструктуры полимерной матрицы. Комплексы металлов с ионитами в ряде случаев моделируют металлсодержащие ферменты. [13]
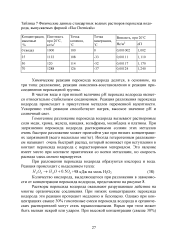 |
Физические данные стандартных водных растворов пероксида водорода, выпускаемых фирмой Eka Chemicals. [14] |
В чистом виде и при низкой величине рН пероксид водорода является относительно стабильным соединением. Реакция разложения пероксида водорода происходит в присутствии металлов переменной валентности. Ускорению этой реакции способствуют нагрев, высокое значение рН и солнечный свет. [15]
Страницы: 1 2