Реакция - разложение - соль
Cтраница 1
Реакции разложения соли или возгонку проводят в пробирках из тугоплавкого стекла, в фарфоровых и металлических чашках или тиглях. [1]
Напишите уравнение реакции разложения соли, при нагревании которой образуется одно простое вещество и два сложных. [2]
Окислы могут также получаться и в результате реакций разложения солей и других сложных веществ. [3]
В 1942 г. одним из авторов настоящей статьи [1] было высказано предположение, что реакции разложения солей диазония можно классифицировать следующим образом. [4]
Интересные результаты были получены Реутовым, Марковской и Мардалейшвили 30 ] при изучении кинетики реакции разложения двой-лых солей типа XC6H4SbCl4 УСбН4Н2С1 железом в ацетоне. [5]
Реакции окрашивания пламени и получение окрашенных перлов проводят с небольшим количеством вещества, которое вносят на платиновой или нихромовой проволоке в пламя газовой горелки или паяльной трубки. Реакции разложения соли или возгонку проводят в пробирках из тугоплавкого стекла, в фарфоровых и металлических чашках или тиглях. [6]
В лабораторной практике эту реакцию проводят, постепенно добавляя холодный раствор соли арендиазония к горячему раствору хлорида одновалентной меди. Реакция разложения соли диазония в присутствии Cu2 ( CN) 2 идет на холоду, а в присутствии бромида одновалентной меди - при комнатной температуре. [7]
На скорость реакции влияют природа веществ, их концентрация, температура, присутствие катализаторов и примесей. Некоторые реакции, например реакции разложения солей серебра, идут под действием света. [8]
Для разложения порошка используют главным образом концентрированную серную кислоту - купоросное масло. Одновременно с основной реакцией проходят реакции разложения солей гомологов уксусной кислоты. Выделяющиеся кислоты отгоняются вместе с уксусной кислотой. В аппарате остается сероватый порошок - окшара, которая является отходом производства. [9]
Одновременно с сульфчтом натрия образуется газообразный хлористый водород. Реагирующую массу нужно нагревать, расходуя ббльшэе количество тепла, так как реакция разложения говаренной соли идет с поглощением тепла. Чем слабее серная кислота, взятая для разложения поваренной соли, тем больше расход тепла вследствие того, что приходится расходовать еще дополнительное тепло на испарение воды, содержащейся в серной кислоте. [10]
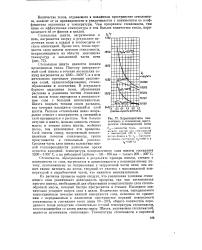 |
Характеристика теплообмена в пламенном пространстве стекловаренной печи. [11] |
Стекольная шихта является плохим проводником тепла. Поэтому поверхностный слой шихты в течение нескольких секунд нагревается до 1200 - 1400 С и в нем интенсивно протекают реакции разложения солей, силикатообразования, стекло-образования и осветления. В результате бурного выделения газов, образования расплава и движения частиц стекловидной массы тепло передается в поверхностном слое с большой интенсивностью. Шихта покрыта тонким слоем расплава, под которым находится спекшийся слой шихты. Расплав стекольная пена непрерывно стекает с поверхности, а спекшийся слой превращется в расплав. Чем больше летучих в шихте, меньше вязкость стекломассы и тоньше помол шихты, особенно песка, тем интенсивнее эти процессы. Слой шихты снизу, нагреваемый конвекционным потоком стекломассы, также превращается в стекольный расплав. [12]
Что же касается реакций соединения и разложения, то они могут быть окислительно-восстановительными, но могут и не быть. Например, реакции образования солей ( СаСО3) из основного и кислотного оксидов ( соответственно СаО и СО2) не являются окислительно-восстановительными. То же относится и к реакциям разложения солей на основной и кислотный оксиды, кислот - на ангидрид и воду и оснований - на основной оксид и воду. [13]
Это соединение реагирует с алкилгалогенидами с образованием ненасыщенных углеводородов и трифенилгалогенидов олова, а с ацетилхлоридом - с образованием ацетофенона. При нагревании с серой оно дает дифенилсульфид и дифенилди-сульфид. Гейн и его сотрудники 6 считают, что нейтральные фенильные радикалы выделяются при реакциях разложения солей пентафенилхрома ( С6Н5) 5СгХ, являющихся важными восстановителями и легко теряющих одну фенильную группу. [14]
Кроме того, было установлено, что добавление инертных солей незначительно изменяет скорость процесса. Последующие исследования, выполненные в более концентрированных растворах [18, 19], показали также небольшое влияние на кинетику реакции разложения солей и сильных кислот. Однако этими эффектами обычно можно пренебречь, так что сомнительно, был ли действительно обнаружен кислотный катализ в водном растворе. Большинство экспериментов Бренстед и Педерсен проводили в буферных растворах, приготовленных из слабых кислот. [15]
Страницы: 1 2