Реакция - каталитическое разложение
Cтраница 1
Реакция каталитического разложения НгОа в водном растворе протекает как реакция первого порядка. Константа скорости ее при данных условиях температуры, концентрации и вида катализатора равна k - 0 0437 мин. [1]
К реакциям каталитического разложения углеводородов относится также каталитический крекинг, имеющий исключительно большое промышленное значение. Так, в США с его помощью получено в 1953 г. около 135 милл. [2]
Многократные исследования реакции каталитического разложения перекиси водорода с применением теории активных ансамблей Кобозева показали, что наиболее активным центром в этой реакции является атом платины. [3]
Из уравнения реакции каталитического разложения бертолетовой соли ( см. решение 5) видно, что 3 г-моль О2 выделяется при разложении 2 г-моль КСЮ3, а 0 9 г-моль 02 выделится при разложении 0 6 г-моль КСЮ3 в результате чего образуется 0 6 г-моль, или 0 6 74 5 44 7 г, КС. Остальные 0 6 г-моль ( 1 2 - - 0 6 0 6) бертолетовой соли разлагаются с образованием перхлората и хлорида калия. Значит, в остатке содержится 62 325 г перхлората калия и 55 875 г ( 44 7 11 175 55 875) хлорида калия. [4]
Более обстоятельное исследование реакции каталитического разложения гидразина было осуществлено Гутбиром и его сотрудниками [178], которые изучали также действие платиновой черни. Ниже суммированы результаты этой работы. [5]
Колебательные изменения в процессе реакции каталитического разложения пероксида водорода в присутствии Ре ( МО3) з - 9Н2О в азотнокислом растворе, происходящей в ППР, были изучены в работе Виргеса [219] и определены критические значения скорости реакции, которые приводят к колебаниям температуры и конверсии. Сравнение экспериментальных значений с результатами расчетов показывают большие отклонения рассчитанных величин амплитуды колебаний температуры от экспериментальных. Лучшее совпадение теории с экспериментом было получено при использовании более совершенной модели, учитывающей выпаривание воды. [6]
Рассмотрим, например, реакцию каталитического разложения аммиака на металлах. Принято считать, что этот процесс контро-руется десорбцией азота, адсорбированного на поверхности катализатора. [7]
Учет реакций нулевого цикла, реакций каталитического разложения О3, процессов диффузии позволил построить расчетный график [ О3 ] / ( Z), рис. В-21, практически совпадающий с данными натурных измерений [ О3 ] в мезо-и стратосфере. Уменьшение [ О3 ] при Z 30 км определяется уменьшением скорости генерации атомов кислорода из О2, поскольку мала становится интенсивность фотоактивного света / с X 240 нм. Отклонение [ О3 ] / ( Z) в большую сторону при Z 15 км связано с образованием О3 в результате окисления органических веществ, поступающих в атмосферу с поверхности Земли. [8]
Следует еще упомянуть о новейших исследованиях реакции каталитического разложения перекиси растворами псрмат ь пата. Согласно Фуина, при постоянной концентрации псрман - iаната l 15 - lft мол / я разложение перекиси в пределах кЪнцеп - граций от 0 0173 до 0 469 мол. [9]
На рис. 1 представлены кинетические кривые для реакции каталитического разложения кумола над обезвоженным катализатором АС-69 и над тем же катализатором после введения в реактор воды. [10]
На рис. 1 представлены кинетические кривые для реакции каталитического разложения хумола над обезвоженным катализаторам АС-69 и над тем же катализатором после введения в реактор воды. [11]
Вольф также опубликовал ( 1912 г.) схему реакции каталитического разложения гидразонов с выделением азота, причем методика Вольфа была иной ( реакция проводится в запаянных трубках в присутствии этилата натрия), чем Кижнера. Поскольку открытие новой реакции было сделано двумя авторами независимо друг от друга ( Кижнер, однако, дал ее описание раньше Вольфа на полтора года), она получила название реакции Кижнера - Вольфа. Видоизмененная методика реакции Кижнера разработана Хуан-Минлоном. [12]
В задание входит определение скорости и периода полураспада реакции каталитического разложения перекиси водорода при комнатной температуре. [13]
Довольно часто применяется медь и ее аналоги в реакциях каталитического разложения. Здесь наиболее характерны два типа процессов: первый из них - разложение диазосоедине-ний при низких температурах [194, 245, 251-253, 320-334, 973, 974, 977, 1235, 1236], часто сопровождающееся полимеризацией раднкалоподобных продуктов первичного распада или их присоединением по кратным связям других молекул, присутствующих в реакционной смеси. [14]
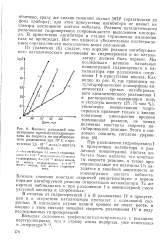 |
Влияние начальной концентрации т / е / й-бутилгидропере-киси на скорость ее ингиб. ирован-ного разложения при 70 С в присутствии 2 5 10 моль / л ацетата кобальта. [15] |
Страницы: 1 2 3