Реакция - рацемизация
Cтраница 2
Этилсульфокислота даже при температуре 102 - 106 очень слабо действует на реакции рацемизации, водородного обмена и изомеризации - 3-метилгептана. [16]
Простейший метод изучения стереохимии карбанионов состоит в сравнении относительных скоростей катализируемых основаниями реакций рацемизации и водородного обмена для оптически активных С - Н - кислот. Найдено, что максимальная величина удельного вращения практически одинакова для дейтерирован-ных и недейтерированных С - Н - кислот. [17]
Хлористый водород, хлористый литий и хлористый тетраметиламмо-ний не являются катализаторами ни для реакции рацемизации, ни дли реакции алкилирования. [18]
Это становится ясным при количественном исследовании устойчивости атропизомеров, например путем определения энергии активации реакции рацемизации. [19]
Взаимное превращение энантиомеров не является вырожденной реакцией, если рассматривать отдельные молекулы, но при учете всей массы молекул реакция рацемизации dl ч Id становится вырожденной. [20]
Эти лиганды могут образовывать диссимметричные тетраэдрические комплексы, которые находятся в быстром равновесии с диамагнитной плоской квадратной конфигурацией, но инертны в реакции рацемизации. Инертность возникает вследствие того, что лиганд, который сам может быть расщеплен на оптически активные изомеры, инертен к инверсии из-за ограниченного вращения замещенного бифенила. Две энантиомер-ные конфигурации показаны на рис. 6 - 42 и помечены s и R ( Д и Л [54]), согласно правилам, приведенным в гл. Поскольку известно, что конфигурации d - и / - 2 2 -диамино - 6 6 -диметилдифенила обозначаются буквами R и s соответственно [50], абсолютные конфигурации комплексов, образованных основаниями Щиффа этого диамина, однозначно определены. [21]
Подставляя в соотношения (3.53) - (3.54) численные значения кинетических и равновесных констант, а также значения [ Н ] и [ ОН - ] из условия задачи, найдем величины скоростей реакций рацемизации. [22]
Таким образом, приходится констатировать, что рассмотренные исследования не дали пока однозначного ответа на вопрос об относительной роли перекрывания ван-дер-ваальсовых сфер несвязанных атомных групп и деформации связей при образовании активированного комплекса в реакциях рацемизации. Дальнейшее изучение этих и других модельных реакций под высоким давлением представляется весьма целесообразным. [23]
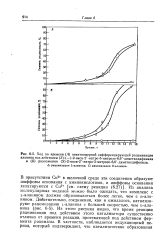 |
Ход во времени ( А энантиомернои дифференцирующей рацемизации. [24] |
Из анализа молекулярных моделей можно было ожидать, что комплекс с ь-аланином должен образовываться более легко, чем с о-ала-нином. Из этого рисунка видно, что время реакции рацемизации под действием этого катализатора существенно отлично от времени реакции, протекающей под действием фермента рацемазы. [25]
Другие данные также подтверждают механизм SN. Скорость реакции такая же, как скорость реакции рацемизации, если используется оптически активный zfuc - Co ( en) 2Clg, что должно быть только в том случае, если интермедиат является симметричным или существует достаточно долго. [26]
Значительно меньше имеется примеров неферментативных реакций в растворе, в которых скорость реакции возрастает за счет индуцирования напряжения в субстрате при связывании с катализатором. Образование комплекса между асимметрическим субстратом и плоским катализатором облегчает образование планарного переходного состояния, которое требуется для реакции рацемизации. [27]
Со ( ПГ) от Со ( еп) з до Со ( С204) з делает их более лабильными к фото - ( и термическому) восстановительному разложению, а также к фото - ( и термической) рацемизации. Такое поведение подтверждает точку зрения Адам-сона [216], который считает, что фотолабилизация комплексов Со ( Ш) по отношению к реакциям рацемизации ( и аквотации), по-видимому, тесно связана с легкостью окисления ацидогрупп и, следовательно, с легкостью фотовосстановительного разложения. [28]
Общие пути превращения аминокислот включают реакции дезаминиро-вания, трансаминирования, декарбоксилирования, биосинтеза и рацемизации. Рассмотрим подробно первые четыре реакции, имеющие значение для всех живых организмов. Реакции рацемизации характерны только для микроорганизмов; открыты ферменты, катализирующие рацемизацию ряда аминокислот ( Ала, Глу, Про, Мет, Лиз, Сер) и эпимеризацию оксипролина и а е-диаминопимелиновой кислоты. Физиологическая роль рацемаз микроорганизмов сводится, вероятно, к синтезу D-изомеров аминокислот для построения клеточной оболочки. [29]
Скорость потери оптической активности водных растворов этих соединений варьируется от исключительно высокой до исключительно низкой. Во многих случаях скорость такова, что она не может быть определена обычными методами. Реакции рацемизации - частный случай реакций изомеризации и обычно являются также реакциями замещения или обмена. Близость этих процессов иллюстрируется тем, что в этой главе часто приходилось ссылаться на реакции рацемизации в связи со стереохимией реакций замещения и изомеризации. В этом разделе приведено несколько примеров реакций с различными типами механизмов рацемизации. Такие механизмы реакций удобно классифицировать и обсуждать как внутри - или межмолекулярные. [30]
Страницы: 1 2 3