Реакция - связывание
Cтраница 1
Реакция связывания растворенного в воде кислорода гидратом закиси марганца и переход в гидрат окиси марганца протекает достаточно быстро; по мере уменьшения концентрации кислорода реакция замедляется и, когда остаются следы растворенного в воде кислорода, она протекает медленно. Кроме того, получающийся осадок марганца очень рыхлый и оседает на дно постепенно. Как правило, уже через 40 - 60 мин осадок почти полностью оседает на дно. После указанного или более длительного срока приступают к растворению осадка и титрованию освобождающегося свободного йода. [1]
Реакция связывания водорода фтором имеет важное значение для уменьшения порообразования. При испарении флюсов, содержащих фтористый кальций, и последующем их разложении выделяется фтор, который активно соединяется с имеющимся в зоне дуги водородом; фтористый водород стоек даже при высоких температурах, поэтому в состав флюсов обычно вводят плавиковый шпат, содержащий значительное количество фтористого кальция. [2]
Реакция связывания растворенного кислорода вышеуказанными реагентами производится при наличии избытка щелочей в воде. [3]
Окончание реакции связывания хлор-иона в малорастворимое хлористое серебро определяется по появлению коричнево-красного окрашивания. Объясняется это выпадением осадка двухромовокисло-го серебра при введении в раствор иона серебра в количестве, большем, чем связываемое содержащимся в воде хлор-ионом. [4]
Скорость реакции связывания окиси магния хромитом в различной степени зависит от величины зерен этих веществ. [5]
В реакциях связывания фермента с субстратом ион металла часто нейтрализует отрицательные заряды анионных групп. [6]
Константа скорости реакции связывания окислов в твердый раствор зависит не только от температуры и природы изучаемого окисла, но и от наличия в смеси других окислов. [7]
 |
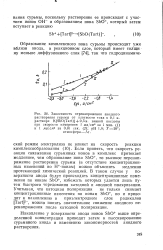
Технологическая схема промышленной установки для очистки сырого аргона от кислорода с помощью меди. [8] |
В результате реакции связывания кислорода при окислении меди температура аргона в реакторе ( и меди соответственно) повышается до 400 - 550 С. [9]
Увеличить выход в реакции связывания можно, повысив рН и температуру реакции. [10]
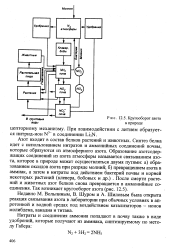 |
Кругооборот азота в природе. [11] |
Шиловым была открыта реакция связывания азота в лаборатории при обычных условиях в ап-ротонной и водной средах под воздействием катализаторов - ионов молибдена, ванадия и титана. [12]
При 1223 - 1373 К реакции связывания СаО в присутствии 0 1 - 3 % P2Os протекают несколько интенсивнее, чем без него, вследствие образования фосфатов кальция. В присутствии Р5 снижается энергия активации процессов разложения природных минералов и синтеза первичных соединений. Однако уже вьцде 1423 К наблюдается замедление реакций минералообразования, что следует связать с образованием трудноразлагающихся фосфорсодержащих промежуточных соединений. [13]
Методы комплексообразования основаны на применении реакций связывания ионов в прочные комплексные соединения. [14]
Страницы: 1 2 3 4