Реакция - взаимодействие - радикал
Cтраница 2
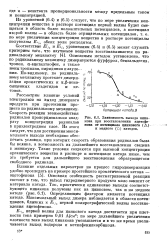 |
Зависимость выхода пинакона при восстановлении ацетофенона от потенциала цинкового Д - и медного ( О катодов. [16] |
Рассмотрим влияние условий электролиза на выход димерного продукта при протекании процесса по радикальному механизму. Скорость реакции взаимодействия радикалов пропорциональна квадрату концентрации радикалов в приэлектродном слое. Из этого следует, что для достижения максимального выхода необходимо обеспечить условия, при которых скорость образования радикалов была бы велика, а возможность их дальнейшего восстановления сведена к минимуму. Такие условия создаются при высокой концентрации органического вещества в растворе и потенциале катода ниже, чем это требуется для дальнейшего восстановления образующегося свободного радикала. [17]
Скорость сополимеризации и молекулярный вес сополимера лишь незначительно зависят от гх и г2, но существенным образом определяются механизмом реакции обрыва цепей. По данным о скоростях сополимеризации может быть рассчитана скорость реакции взаимодействия радикалов Р и Q, единственная неизвестная величина в кинетическом уравнении. Для многих систем было показано, что скорость сополимеризации не является линейной функцией состава мономерной смеси, а равна гораздо меньшей величине. Соответствующим образом уменьшаются и молекулярные веса сополимеров. Можно ожидать, что константа скорости взаимодействия радикалов Р nQ должна быть равна среднему геометрическому из констант скоростей раздельного обрыва радикалов Р и Q при предположении о том, что в таких реакциях, обладающих практически нулевой энергией активации, каждый радикал обладает определенной, присущей ему реакционной способностью. Такое простое соотношение наблюдается при сополимеризации стирола и п-метокси-стирола. [18]
Поперечные связи возникают в результате рекомбинации, образующихся под действием излучения полимерных радикалов. Однако определенную роль в этом процессе могут играть также ионно-молеку-лярные реакции и реакции взаимодействия радикалов с функциональными группами с двойными связями и с возбужденными молекулами. [19]
Расчеты также показывают, что с точки зрения термодинамики более вероятен процесс с образованием амидных радикалов, который идет с меньшим повышением энергии Гиббса системы, чем процесс с появлением имидного радикала. Реакция ди-меризации амидных радикалов протекает с большим понижением энергии Гиббса и выделением тепла, чем реакция взаимодействия имидного радикала с молекулой аммиака. Так как гидразин менее устойчив, чем аммиак, то образование гидразина возможно лишь при его немедленном удалении из зоны реакции. [20]
Как уже сказано, одним из процессов, приводящих к обрыву цепи, является захват свободных радикалов стенкой. Процесс обрыва цепи в этом случае является гетерогенным и складывается из двух процессов: а) диффузии радикалов к стенке и б) захвата радикала стенкой. Более медленный из этих процессов определяет скорость всего процесса в целом. Если медленным процессом является диффузия, то процесс обрыва цепи называется диффузионным; его скорость определяется скоростью диффузии свободных радикалов к стенке. Если же медленным процессом является реакция взаимодействия радикалов со стенкой, то скорость обрыва определяется этой скоростью и не зависит от скорости диффузии. Таким образом, лимитирующей стадией является кинетическая стадия, и обрыв называется кинетическим обрывом. В этом случае происходит более тысячи соударений атома или радикала со стенкой, прежде чем произойдет его гибель. [21]
Рассмотрим возможные пути участия молекул ингибиторов в образовании продуктов окисления углеводородов. Так как при радиолизе возникают заряженные частицы, возбужденные молекулы и радикалы, то необходимо рассмотреть все возможные реакции. Если бы молекулы ингибиторов дифениламина и ионола участвовали как акцепторы заряженных частиц или возбуждения, то повышение концентрации ингибиторов в углеводородах должно было привести к понижению выхода соответствующих алкилгидроперекисеи, при этом должны были бы образовываться гидроперекиси из ингибиторов. При радиационном окислении н-гептана в присутствии ионола гидроперекись ионола не была обнаружена. Это показывает, что наиболее вероятна реакция взаимодействия радикалов RO2 с молекулами ингибитора. [22]
Страницы: 1 2