Реакция - синтез - карбамид
Cтраница 1
Реакция синтеза карбамида открыта русским ученым А. И. Базаровым еще в 1868 г., когда он защитил диссертацию на тему Прямое получение мочевины из углекислоты и аммиака. [1]
Однако реакция синтеза карбамида всегда протекает через образование промежуточного продукта - карбамата аммония с последующей дегидратацией его в карбамид. Степень превращения карбамата в карбамид и количественный состав плава, выходящего из колонны синтеза, могут быть неодинаковыми в различных схемах. [2]
Вопрос о стадийности реакции синтеза карбамида сначала обсуждался в работе [22], где была выдвинута гипотеза о протекании этой реакции через промежуточное образование циановой кислоты путем дегидратации карбаминовой кислоты. [3]
Это подтверждает гетерогенность продуктов реакции синтеза карбамида и ее протекание в жидкой фазе. [4]
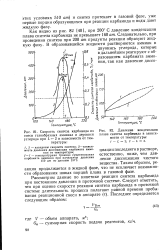 |
Скорость синтеза карбамида из смеси газообразных аммиака и двуокиси углерода при L 2 в зависимости от температуры.| Давление конденсации плава синтеза карбамида в зависимости от температуры. [5] |
Рассмотрим данные по кинетике реакции синтеза карбамида при постоянном давлении в проточной системе. [6]
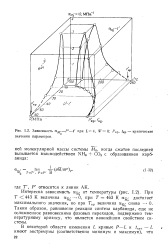 |
Зависимость а. м - Р - f при L4, W 0. Ркр, tKp - критические значения параметров. [7] |
Таким образом, равновесие реакции синтеза карбамида, еще не осложненное равновесиями фазовых переходов, подвержено температурному кризису, что является важнейшим свойством системы. [8]
Как известно [1,52,53], инертные по отношению к реакции синтеза карбамида газы, практически не растворимые в жидкой фазе, снижают степень превращения сырья в карбамид. [9]
Параметрическое уравнение (1.14) в неявной форме отражает глубину протекания реакции синтеза карбамида в жидкой фазе. [10]
Компоненты формально тождественны веществам, смешение которых при определенных условиях приводит к реакции синтеза карбамида, но в брутто-форме представляют все многообразие реально существующих молекул ( в том числе и молекулу карбамида) ионов, ассоциатов, возникающих по достижении равновесия процесса. [11]
 |
Зависимость ж -. при t 190 С, W 0 и рк а 0 226 г / см3. [12] |
Рассматриваемые исследования [3, 4], очевидно, приобретут важное прикладное значение, когда будут найдены доступные и эффективные средства удаления Н2О из зоны реакции синтеза карбамида. [13]
Плавкость в четырехкомпонентной системе карбамид-вода - аммиак-двуокись углерода исследовали Денис и Блек [38], которые во всех опытах поддерживали мольное отношение Шсо ( мн ь: : Щцг0 1, что отвечает стехиометрии реакции синтеза карбамида. [14]
Основные недостатки промышленных методов выделения непрореагировавших веществ из плава синтеза карбамида и их рециркуляции в схемах с жидкостным рециклом - высокое содержание воды в смеси реагентов на входе в колонну синтеза, недостаточная степень отгонки МН3 и СО2 на I ступени дистилляции, сложность обслуживания карбаматных насосов, необходимость испарения на стадиях дистилляции и выпарки значительного количества воды сверх стехиометрической нормы ( по реакции синтеза карбамида) и др. В результате ограничиваются возможности интенсификации производства, требуются повышенные энергетические и трудовые затраты. [15]
Страницы: 1 2