Реакция - угль
Cтраница 3
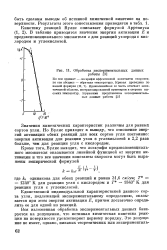 |
Обработка экспериментальных данных работы. [31] |
Значения кинетических характеристик различны для разных сортов угля. Но Вулис приходит к выводу, что отношение энергий активации обеих реакций для всех сортов угля постоянно: энергия активации для реакции угля с углекислотой в 2 2 раза больше, чем для реакции угля с кислородом. [32]
Таким образом, катализатор перемещается в реакционной аппаратуре, плавает в сырье и выводится из процесса вместе с продуктами реакции. При гидрогенизации углей, которые всегда содержат значительное количество золы, катализатор смешивается с этой золой и остатками не вступившего в реакцию угля, причем содержание катализатора в общем твердом остатке оказывается сравнительно небольшим. Поэтому нецелесообразно возвращать остаток в процесс для вторичного использования. В то же время регенерация катализатора из остатка очень затруднительна. [33]
Таким образом, катализатор перемещается в реакционной аппаратуре, плавает в сырье и выводится из процесса вместе с продуктами реакции. В случае гидрогенизации углей, которые всегда содержат значительное количество золы, катализатор смешивается с этой золой и остатками не вступившего в реакцию угля, причем содержание катализатора в общем твердом остатке оказывается сравнительно небольшим. Поэтому нецелесообразно возвращать остаток в процесс для вторичного использования. В то же время регенерация катализатора из остатка очень затруднительна. [34]
 |
Обработка экспериментальных данных. [35] |
Значения кинетических характеристик различны для разных сортов угля. Но Вулис приходит к выводу, что отношение энергий активации обеих реакций для всех сортов угля постоянно: энергия активации для реакции угля с углекислотой в 2 2 раза больше, чем для реакции угля с кислородом. [36]
По наиболее распространенному способу ( см. разд. Альтернативные способы основаны на реакции угля с воздухом и паром с получением низкокалорийного газа ( 5580 - 7440 кДж / м3) и реакции с водородом ( гидрогазификации) для максимального увеличения: выхода метана. [37]
 |
Схема распределения температурных зон в бескерновой печи ( вертикальный разрез. [38] |
Шихта в бескерновой печи располагается в трех основных зонах. В центральной высокотемпературной зоне / / / реакция восстановления окиси бора проходит до конца. Промежуточная зона / / после окончания процесса заполнена смесью, состоящей главным образом из карбида бора, остатков не вступившего в реакцию угля, недовосстановленной окиси бора и, возможно, низших оксидов бора. Наружная зона / заполнена почти не измененной исходной шихтой, которая во время процесса служит теплоизоляцией. [39]
Значительная часть мировой потребности в энергии удовлетворяется непосредственно или косвенно путем использования реакций угля и углеродсодержащих материалов с газами. Наиболее важными являются реакции с кислородом, водяным паром, двуокисью углерода и водородом. Экзотермическая реакция угля с кислородом служит главным источником получения энергии во всем мире. Эндотермическая реакция угля с водяным паром дает окись углерода и водород, которые используются либо непосредственно как газообразное топливо, либо в виде синтез-газа, превращаемого каталитическими методами в ряд углеводородных топлив или в органические химикалии. Так как двуокись углерода является непосредственным продуктом реакции угля с кислородом и вторичным продуктом реакции угля с водяным паром, получающимся по реакции конверсии водяного газа, вторичная реакция двуокиси углерода с углем в слое топлива тесно связана с первичными реакциями углерода с газами. Реакция водорода с углем, приводящая к образованию метана, в настоящее время не имеет большого промышленного значения, но в будущем найдет, по-видимому, широкое применение. [40]
Значительная часть мировой потребности в энергии удовлетворяется непосредственно или косвенно путем использования реакций угля и углеродсодержащих материалов с газами. Наиболее важными являются реакции с кислородом, водяным паром, двуокисью углерода и водородом. Экзотермическая реакция угля с кислородом служит главным источником получения энергии во всем мире. Эндотермическая реакция угля с водяным паром дает окись углерода и водород, которые используются либо непосредственно как газообразное топливо, либо в виде синтез-газа, превращаемого каталитическими методами в ряд углеводородных топлив или в органические химикалии. Так как двуокись углерода является непосредственным продуктом реакции угля с кислородом и вторичным продуктом реакции угля с водяным паром, получающимся по реакции конверсии водяного газа, вторичная реакция двуокиси углерода с углем в слое топлива тесно связана с первичными реакциями углерода с газами. Реакция водорода с углем, приводящая к образованию метана, в настоящее время не имеет большого промышленного значения, но в будущем найдет, по-видимому, широкое применение. [41]
Даже несмотря на то что реакции угля с газами используют ся в промышленности в течение многих лет, понимание основ механизма и кинетики реакций сильно отставало от их практического использования. В первую очередь это было вызвано отсутствием экспериментальной техники для определения свойств одного из реагентов - угля. Появление относительно недавно возможностей количественного определения таких свойств твердых тел, как величина поверхности, распределение пор, кристаллографические параметры, средние размеры кристаллитов, электронные свойства, а также возможностей измерения хемосорбции газов, следов примесей, скорости переноса газа в порах, способствовало более ясному пониманию реакций углерода с газами. Исследователи в области катализа, пользовавшиеся перечисленными экспериментальными методиками для описания применявшихся ими катализаторов, за последние годы достигли больших успехов в выяснении реакций, происходящих на поверхности твердых тел. Поэтому многие из развитых ими концепций были использованы авторами настоящей статьи и другими исследователями, изучающими реакции углей с газами. Желательно, чтобы такие теоретические положения нашли еще более широкое применение. С учетом этой главной цели и была написана данная статья. [42]
Страницы: 1 2 3