Реакция - восстановление - анион
Cтраница 1
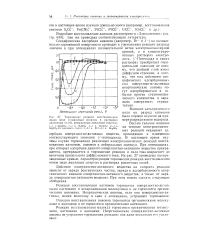 |
Торможение реакции восстановления ионов меди я-амиловым спиртом в растворах различных солей, насыщенных амиловым спиртом. [1] |
Реакции восстановления анионов тормозятся органическими молекулами и анионами и не тормозятся органическими катионами. [2]
Скорость реакции восстановления анионов возрастает с увеличением концентрации органического катиона, длины органического радикала, заряда органического катиона. Увеличение скорости восстановления исследованных анионов в присутствии органических катионов в соответствии с уравнением ч (5.45) связано с уменьшением отрицательных значений i-потенциала и указывает на преобладание электростатических эффектов над другими ингибирующими эффектами. Скорость стадии разряда при электровосстановлении анионов в присутствии органических катионов определенной концентрации может возрасти настолько, что при измерениях на капельных и вращающихся дисковых электродах дальнейшее возрастание тока прекращается, поскольку общая скорость реакции определяется уже медленностью диффузионной стадии. В этих условиях невозможно однозначно установить, связан ли каталитический эффект органических катионов только с изменением - фгпотенциала. [3]
Органические катионы ускоряют реакцию восстановления анионов, а органические анионы тормозят электродный процесс. Различное действие адсорбированных органических ионов указывает на то, что их влияние связано в основном с изменением - потенциала. Влияние неорганических и органических катионов на скорость реакции восстановления аниона персульфата наблюдается только в области потенциалов их адсорбции. [5]
При потенциалах десорбции ПАОВ ток реакции восстановления анионов возрастает до значений, отвечающих разряду в растворах без добавок ПАОВ. [6]
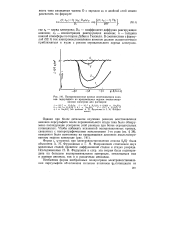 |
Поляризационные кривые восстановления анионов персульфата на вращающемся медном амальгамированном электроде для растворов. [7] |
Однако при более детальном изучении реакции восстановления анионов персульфата после первоначального спада тока было обнаружено последующее ускорение этой реакции при более отрицательных потенциалах. [8]
В работах Н. В. Николаевой-Федорович рассмотрено влияние адсорбированных ПАВ на реакции восстановления анионов и окисления катионов. Результаты, полученные в этих и некоторых других исследованиях, полностью подтверждают электростатический характер действия ПАВ на кинетику реакции восстановления. Рассматривая влияние Wi потенциала на скорость реакции, следует заметить, что основная часть ионов расположена во внешней плоскости Гельмгольца и в диффузном слое, однако имеется некоторое количество ионов, которые находятся во внутренней области Гельмгольца и непосредственно соприкасаются с поверхностью электрода. Было показано, что именно эти ионы и участвуют в разряде. [9]
В разбавленных растворах фона при д 0 /, с-кривые реакции восстановления анионов искажены полярографическим максимумом 1-го рода, что не позволяет исследовать кинетику этих процессов. [11]
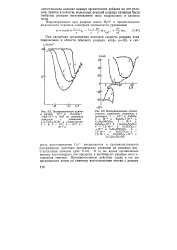 |
Поляризационные кривые в системе 10 - 3 н. Na2S2Og.| Поляризационные кривые ртутного капельного электрода в. [12] |
В то же время органические анионы катализируют эти процессы и ингибируют реакции восстановления анионов. [13]
Из этого уравнения следует, что и для реакции окисления катионов аналогично реакции восстановления анионов первой группы поляризационная кривая в разбавленных растворах имеет сложную форму с максимумом тока при qG и минимумом при 70, причем скорость реакции зависит от о - потенциала, величина и знак которого определяются составом раствора и потенциалом электрода. [14]
Органические анионы, например анионы алкилсульфокислот предельного ряда, при адсорбции на электроде увеличивают отрицательное значение - потенциала, что приводит к ингибированию реакции восстановления анионов первой группы. В соответствии с уравнением (5.46) органические анионы ускоряют реакцию окисления европия, что указывает на электростатический характер их действия. [15]
Страницы: 1 2