Реакция - выделение
Cтраница 2
Раствор будет готов после прекращения реакции выделения пузырьков газа, станет прозрачным. [16]
Простой метод определения хлора основывается на реакции выделения иода под действием хлора из иодида калия в среде разбавленной серной кислоты. [17]
 |
Прибор для определения фотосинтеза растений при помощи радиоактивного углерода С14 ( 2 - й вариант. [18] |
В этом бюксе в дальнейшем осуществляется реакция выделения газообразной углекислоты. Нижний конец второй трубки должен быть более длинным, чтобы ток воздуха, обогащенного СОа, проходил через весь объем бутыли. [19]
В широком интервале плотностей тока скорость реакции выделения Н2 описывается уравнением Тафеля. При плотностях тока меньших, чем 10 - 4 - 10 А / см2, зависимость изменения потенциала от плотности тока является линейной. [20]
В широком интервале плотностей тока скорость реакции выделения Н2 описывается уравнением Тафеля. При плотностях тока меньших, чем 10 - 4 - 10 - 5 А / см2, зависимость изменения потенциала от плотности тока является линейной. [21]
В широком интервале плотностей тока скорость реакции выделения Н2 описывается уравнением Тафеля. При плотностях тока меньших, чем 10 - 4 - 10 А / см2, зависимость изменения потенциала от плотности тока является линейной. [22]
Поляризационные измерения показали, что скорость реакции выделения ci, на таких анодах отличается примерно во столько же раз во сколько раз изменяется их истинная площадь поверхности. [23]
Ввиду специфичности и некоторых других особенностей реакции выделения газообразных веществ имеют большое значение и в количественном анализе. Содержание воды в разнообразных продуктах обычно определяют удалением Н2О в виде газообразной фазы. Количество воды рассчитывают на основании потери в весе; иногда выделяющуюся воду поглощают каким-либо подходящим веществом, и количество воды определяют по увеличению веса этого вещества. [24]
Ввиду специфичности и некоторых других особенностей реакции выделения газообразных веществ имеют большое значение и в количественном анализе. Содержание воды в разнообразных продуктах обычно определяют путем удаления Н2О в виде газообразной фазы. Количество воды рассчитывают на основании потери в весе; иногда выделяющуюся воду поглощают каким-либо подходящим веществом, и количество воды определяют по увеличению веса этого вещества. [25]
Для открытия иона ртути часто применяют реакцию выделения ртути при помощи металлической меди. [26]
При малых содержаниях мышьяка его открывают по реакции выделения металлического золота: небольшое количество раствора подщелачивают едким натром и вводят крупинку сплава Деварда; выделяющийся мышьяковистый водород улавливают фильтровальной бумагой, смоченной раствором хлорида золота, которое при этом восстанавливается до металлического, давая черное или синеватое пятно в зависимости от содержания иона мышьяка. [27]
 |
Изменение вероятности выделения углерода при конверсии метана водяным паром. ( См. пример 18.| Влияние температуры. [28] |
Хотя повышение температуры увеличивает вероятность и скорость реакции выделения углерода, оно одновременно ускоряет реакцию взаимодействия СН4 и Н2О, вследствие чего понижается концентрация СН4, и уменьшается вероятность, а вместе с тем и скорость выделения углерода. [29]
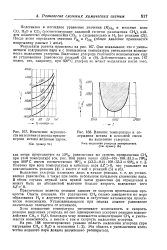 |
Изменение вероятности выделения углерода при конверсии метана водяным паром.| Влияние температуры и содержания метана в исходной смеси на выделение углерода. [30] |
Страницы: 1 2 3 4