Реакция - гидроксиламин
Cтраница 2
 |
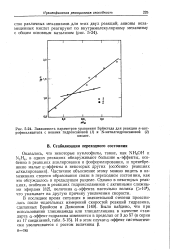
Вычисленные значения констант скорости второго порядка для реакции аденозина с гидроксиламином и О-метилгидрохсиламином 163. [16] |
В табл. 5.3 приводятся величины констант скорости реакции второго порядка, вычисленные для реакции гидроксиламина и О-метилгидроксил-амина с аденозином. [17]
Предложенный механизм реакции гидроксиламина с цитидином сходен с механизмом, выдвинутым для объяснения реакции гидроксиламина с 3-метилцитозином ( см. стр. [18]
Образование / г-нитрофенолят-иона ( по Ямакс 400 ммк) и гидроксамовой кислоты [ по цветной реакции с Fe ( III) при 545 ммк ] в реакции гидроксиламина с л-нитрофенилацетатом в водном растворе при постоянном значении рН можно проследить в отдельности, поэтому константы скорости и рН - зависимости первой и второй стадий могут быть получены независимо друг от друга. [19]
Нуклеофилы, в молекуле которых отщепляющаяся группа ( ОН, N2, N02) связана с атомом азота, могут образовать азиридины. В реакциях гидроксиламина [211 - 213], азотистоводородной кислоты [214] и нитрамина [215] с различными ненасыщенными соединениями получаются обычные продукты присоединения. Образование азиридина, например, в реакциях фенилазида со стиролом [216] или азида карбамино-вой кислоты с диэтиловым эфиром фумаровой кислоты [217], по-видимому, происходит или благодаря вторичным реакциям первичного продукта, или путем синхронного присоединения с образованием циклов. Катализируемое основаниями образование азиридина из продукта присоединения метоксиламина к халкону [ 42, 45Ь ], по-видимому, протекает по механизму, аналогичному эпоксидированию с отщеплением группы СН. [20]
Нуклеофилы, в молекуле которых отщепляющаяся группа ( ОН, N2, N02) связана с атомом азота, могут образовать азиридины. В реакциях гидроксиламина [211 - 213], азотистоводородной кислоты [214] и нитрамина [215] с различными ненасыщенными соединениями получаются обычные продукты присоединения. Образование азиридина, например, в реакциях фенилазида со стиролом [216] или азида карбамино-вой кислоты с диэтйловым эфиром фумаровой кислоты [217], по-видимому, происходит или благодаря вторичным реакциям первичного продукта, или путем синхронного присоединения с образованием циклов. [21]
Нуклеофильное замещение протекает особенно легко в случае аминосоединений, содержащих электронодонорные заместители, а также в случае гидразинов и гидроксиламлнов. Изучена кинетика реакции гидроксиламина с алкиламидами при 25 С, в которой замещение аминного фрагмента приводит к гидроксамовой кислоте ( см. разд. Кривая зависимости скорости реакции от рН имеет колоколообразную форму, что указывает на общий кислотный катализ гидроксиламмониевым ионом, который, однако, замедляется при высоких концентрациях. [22]
Кинетика образования оксима или семикарбазона изучалась спектро-фотометрически, поскольку поглощение карбонильной группы в области 2700 - 2800 А ( 270 - 280 нм) уменьшается при образовании промежуточного комплекса. В почти нейтральном растворе реакция гидроксиламина с альдегидом ( рис. 15.1) протекает очень быстро, поскольку интенсивность абсорбции быстро уменьшается, причем степень уменьшения изменяется при изменении концентрации основания. Скорость суммарной реакции зависит от концентрации продукта присоединения, который претерпевает дегидратацию в оксим. [23]
А ( 270 - 280 нм) уменьшается при образовании промежуточного комплекса. В почти нейтральном растворе реакция гидроксиламина с альдегидом ( рис. 15.1) протекает очень быстро, поскольку интенсивность абсорбции быстро уменьшается, причем степень уменьшения изменяется при изменении концентрации основания. Скорость суммарной реакции зависит от концентрации продукта присоединения, который претерпевает дегидратацию в оксим. [24]
Окиси азометинов, или нитроны, известны с 1887 г. Существует несколько методов их синтеза. Наиболее удобными являются, очевидно, реакции JV-монозамещенных гидроксиламинов с карбонильными соединениями, дегидрогенирование N N-fmaa - мещенных гидроксиламинов и алкилирование оксимов. [25]
 |
Зависимость параметров уравнения Бренстеда для реакции п-нит-рофенилацетата с ионами гидроксамовой ( / и N-метилгидроксамовой ( 2. [26] |
Однако в некоторых реакциях, особенно в реакциях гидроксиламинов с активными сложными эфирами [82], величина а-эффекта настолько велика ( 10в), что указывает на другую причину увеличения скорости. [27]
Интересной новой реакцией является реакция полиакрилонитрила с гидроксиламином. Реакция эта протекает так же, как и реакция гидроксиламина с низкомолекулярными нитрилами. В результате получается полиакриламидоксим, представляющий собой новый полиамфолит, в котором каждый заместитель является одновременным носителем кислых и основных свойств. Большая реакционная способность этих групп открывает возможность синтеза новых полимераналогов полиакрилонитрила. [28]
Это предположение может вызвать некоторое недоумение, поскольку каждый распад промежуточного соединения приводит к образованию продукта и константа скорости первого порядка для распада промежуточного продукта в реакции, которая подчиняется общему первому порядку, должна быть равна константе скорости всей реакции. Однако существенным является то, что абсолютная скорость изменения концентрации промежуточного соединения, накапливающегося в заметной степени, выраженная в моль / л - мин, является очень небольшой по сравнению со скоростью изменения концентраций реагентов и продуктов. Для реакции гидроксиламина стационарное рассмотрение кинетики реакции можно применить при исследовании реакции в условиях низких значений рН, в которых большая часть гидроксиламина протонирует-ся и но происходит заметного накапливания промежуточного продукта; стационарную кинетику, однако, нельзя использовать для анализа экспериментальных данных при высоких значениях рН, когда концентрация свободного гидроксиламина достаточно высока и способна превратить существенную долю карбонильного соединения в промежуточный продукт присоединения. [29]
Страницы: 1 2