Реакция - гидролиз
Cтраница 1
Реакции гидролиза и регидролиза хлора при повышенной температуре протекают практически мгновенно. [1]
 |
Влияние растворителя на процесс гидролиза дитолилтрихлорэтана. [2] |
Реакция гидролиза изучена главным образом на примере гало-гензамещенны. Однако, в этих условиях гидролиз дитолилтрихлорэта-на протекает с очень малой скоростью. Несмотря на увеличение времени реакции до 20 ч, выход не превышает 10 мол. [3]
Реакции гидролиза являются обратными реакциям нейтрализации. [4]
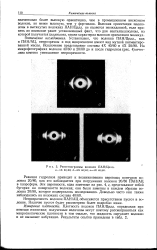 |
Рентгенограммы волокон ПАН / Целл. а - 4Х 80 / 20. 6 - 8Х 60 / 40. в - 4Х 40 / 60. [5] |
Реакция гидролиза приводит к возникновению неровных контуров волокна 20 / 80, как это наблюдается при погружении волокон 20 / 80 ПАН / АЦ в хлороформ. Эти неровности, едва заметные на рис. 4, г, представляют собой бугорки на поверхности волокна; они были заметны в каждом образце волокна 20 / 80, которое подвергалось исследованию. [6]
Реакция гидролиза и гидратации 3CaO - SiO2 является основной реакцией, которая определяет свойства цемента. [7]
Реакция гидролиза наиболее подробно изучена на примерах бензилхло-рида и и-ксилилендихлорида. Оба соединения находят важное применение в качестве промежуточных продуктов органического синтеза, пластификаторов и растворителей. [8]
Реакция гидролиза n - нитрофенилацетата, катализируемая N-метилимидазолом, имеет первый порядок по каждому из реагентов. [9]
Реакция гидролиза идет дальше по уравнению НСО 3 Н2О НгСОз ОН -, но, учитывая наличие в растворе значительного количества ионов ОН -, образующихся при гидролизе соли NaaCOs по первой ступени, гидролиз по второй ступени будет незначительным н им можно пренебречь. [10]
Реакция гидролиза таких солей практически необратима. Реакция среды в таких случаях близка к нейтральной, слабокислой или слабощелочной. [11]
Реакция гидролиза удобна для использования в термохимических исследованиях прежде всего во всех тех случаях, когда в результате этого процесса образуются продукты с известной ( или легко измеряемой) энтальпией образования. Тогда по результатам измерений легко найти энтальпии образования веществ, подвергаемых гидролизу. [12]
Реакции гидролиза обратны реакциям нейтрализации, и поэтому последние идут до конца только при взаимодействии сильных оснований с сильными кислотами. [13]
Реакция гидролиза в этом случае протекает значительно быстрее, чем реакция гидролиза первичных алкильных эфиров, и поэтому считается, что третичные алкильные сложные эфиры обладают неудовлетворительной гидролитической стабильностью. [14]
Реакции гидролиза широко используются в химическом анализе, в частности как характерные реакции в качественном анализе, для поддержания необходимого значения рН в реакциях осаждения и др. Для обнаружения солей аммония используют их способность гидролизоваться с образованием свободного аммиака. [15]
Страницы: 1 2 3 4