Реакция - гидролиз - соль
Cтраница 1
Реакции гидролиза солей характеризуются, помимо константы равновесия, также и константой гидролиза. Константа гидролиза связана с ионным произведением воды и константой диссоциации слабой кис лоты или основания, образующихся в результате гидролиза. Установим эту связь на примере конкретных реакций. [1]
Реакции гидролиза солей характеризуются помимо константы равновесия также и константой гидролиза. Константа гидролиза связана с ионным произведением воды и константой диссоциации слабой кислоты или основания, образующихся в результате гидролиза. Установим эту связь на примере конкретных реакций. [2]
Реакции гидролиза солей многоосновных кислот и многоосновных оснований составляются аналогично, но их следует писать отдельно для. Эти соли гидролизуются по ступеням соответственно ступенчатой диссоциации кислоты или основания. [3]
Реакциями гидролиза солей пользуются нередко для получения гидрозолей оснований и кислот. Таким путем получают золи гидроокисей различных металлов, а также коллоидные растворы кислот. [4]
В результате реакции гидролиза соли образуется осадок основного нитрата ртути Hg ( OH) NO3, pH раствора понижается, раствор приобретает красную окраску. [5]
Написать уравнения реакций гидролиза солей: a) N NOs, б) Mg ( CH3COO) 2 и объяснить, как влияют на гидролиз разбавление раствора и нагревание. [6]
Написать уравнения реакций гидролиза солей: a) NH4NO3, б) Mg ( CH3COO) 2 и объяснить, как влияет на гидролиз разбавление раствора и нагревание. [7]
Написать уравнения реакций гидролиза солей: a) NH4NO3, б) Mg ( CH3COO) 2 и объяснить, как влияет на гидролиз разбавление раствора и нагревание. [8]
Различают три типа реакций гидролиза солей: гидролиз солей слабой кислоты и сильного основания, гидролиз солей сильной кислоты и слабого основания и гидролиз солей слабой кислоты и слабого основания. [9]
Традиционно реакцию взаимодействия ионов соли с водой называют реакцией гидролиза соли. [10]
Традиционно реакцию взаимодействия ионов соли с водой называют реакцией гидролиза соли. [11]
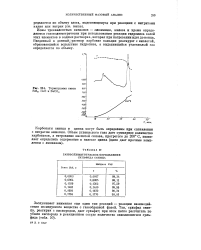 |
Термограмма смеси soo FeS2, CuO и ВаС03 700. [12] |
Ионы трехвалентных катионов - алюминия, железа и хрома определяются газоволюметрически при использовании реакции гидролиза солей этих элементов в водных растворах, которая при нагревании идет до конца. Введенный в данный j раствор карбонат кальция реагирует с кислотой, образовавшейся вследствие гидролиза, а выделившийся углекислый газ определяется по объему. [13]
Реакцию взаимодействия ионов соли с водой, в результате которой образуется слабый электролит, называют реакцией гидролиза соли. Рассмотрим случаи гидролиза солей в общем виде. [14]
Потому что: 1) в состав молекулы входит группа - ОН; 2) протекает реакция гидролиза соли; 3) азот в этом соединении четырехковалентен и не присоединяет ион водорода. [15]
Страницы: 1 2